Способы разделения ионов водорода на поверхности воды

Процесс разделения ионов водорода на поверхности воды играет важную роль в различных химических и физических процессах. Разделение ионов осуществляется с помощью различных способов, включая электролиз, катализаторы и фотоэлектрохимию.
1. Электролиз. Электролиз является одним из основных способов разделения ионов водорода. При электролизе вода разлагается на водород и кислород под воздействием постоянного электрического тока. В результате этого процесса образуются положительные и отрицательные ионы, которые перемещаются к электродам и разделяются.
2. Катализаторы. Разделение ионов водорода на поверхности воды может быть также осуществлено при использовании катализаторов. Катализаторы ускоряют химическую реакцию разделения воды на водород и кислород без участия в самих реакциях. Они обеспечивают более эффективную и быструю разделение ионов на поверхности воды.
3. Фотоэлектрохимия. Фотоэлектрохимический процесс является еще одним способом разделения ионов водорода на поверхности воды. При данном процессе освещенные фотоэлектроды генерируют электрический ток, который приводит к разделению воды на водород и кислород. Этот процесс основывается на использовании фоточувствительных материалов, способных поглощать световую энергию и использовать ее для создания разделения ионов.
Использование указанных способов позволяет эффективно и энергосберегающе проводить разделение ионов водорода на поверхности воды.
Электролиз воды для получения ионов водорода
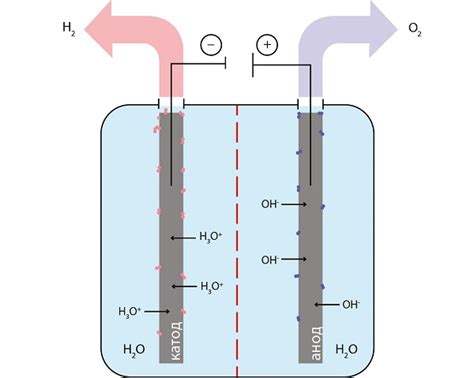
Для проведения электролиза воды необходимы два электрода - анод и катод. Атрибуты катода выбираются из материалов, которые могут образовать молекулы водорода. Часто в роли катода выступает платина или другие редкоземельные металлы.
Когда электрический ток проходит через воду, вода начинает распадаться на ионы водорода и ионы гидроксида. Ионы водорода находятся около катода, где они принимают электроны и становятся атомами водорода (H2). Эти атомы водорода объединяются в молекулы и выходят на поверхность воды, образуя пузырьки газа.
Образующийся при электролизе гидроксидный ион (OH-) соединяется с ионом протона (H+) и образует молекулу воды. Происходит следующая реакция: 2H+ + 2e- = H2
Электролиз воды - это один из способов получения ионов водорода на поверхность воды. Получение ионов водорода в таком виде является важным процессом в различных областях науки и промышленности, включая производство водородных топливных элементов и электролизеры, а также для выделения и очистки водорода.
Основой фотокаталитического разложения воды являются фотокатализаторы - вещества, способные поглощать световую энергию и ускорять химические реакции. Наиболее распространенными фотокатализаторами для разложения воды являются соединения титана, такие как диоксид титана (TiO2).
Процесс фотокаталитического разложения воды происходит следующим образом:
- Под воздействием световой энергии фотокатализатор поглощает фотоны и переходит в возбужденное состояние.
- Возбужденное состояние фотокатализатора способствует разделению молекулы воды на ионы водорода (H+) и кислорода (O2-).
- Свободные ионы водорода реагируют с водой, образуя молекулы водорода (H2).
Преимущества фотокаталитического разложения воды включают низкую стоимость и доступность фотокатализаторов, отсутствие использования вредных реактивов и низкие энергозатраты. Однако, длительность процесса и его эффективность зависят от свойств фотокатализатора, условий освещения и других факторов.
В целом, фотокаталитическое разложение воды представляет собой многообещающий подход к получению ионов водорода на поверхность воды. Продолжаются исследования в области разработки новых фотокатализаторов и оптимизации условий процесса, чтобы достичь более высокой эффективности и применимости этого метода в промышленности и энергетике.