Водород - простейший элемент, который встречается во многих химических соединениях. Знание его массы является ключевым для понимания и расчета реакций, а также для различных научных и инженерных расчетов.
Масса атома водорода выражается в атомных единицах массы (ат.е.), но в ряде случаев может быть необходимо привести ее к единице измерения, более привычной для нас, килограммам. Для этого необходимо знание дефиниции атома водорода в атомных единицах массы и реализация формулы перевода.
Масса атома водорода в атомных единицах массы составляет около 1.008 ат.е.м. В свою очередь, 1 атомная единица массы равна приблизительно 1.661 × 10-27 кг, или 1.661 × 10-24 г.
Теоретические основы

Масса протона является основным вкладом в массу атома водорода. Поэтому массу атома водорода можно приближенно считать равной массе протона. Таким образом, масса атома водорода составляет около 1,67 * 10^-27 кг.
| Частица | Масса (кг) |
|---|---|
| Протон | 1,67 * 10^-27 |
| Электрон | 9,11 * 10^-31 |
Учитывая, что атом водорода состоит из одного протона, его масса в килограммах составляет примерно 1,67 * 10^-27 кг.
Атом водорода и его структура
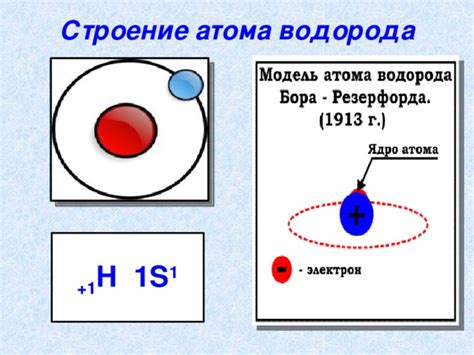
Протон, являющийся положительно заряженной частицей, находится в центре атома и образует ядро. Вокруг ядра электрон находится на определенном расстоянии, двигаясь по орбите. Электрон обладает отрицательным зарядом и компенсирует положительный заряд протона, что делает атом электрически нейтральным.
Структура атома водорода может быть представлена следующим образом:
- Ядро: состоит из одного протона, который определяет химические свойства атома водорода.
- Орбиталь: электрон вращается вокруг ядра по орбите, которая определена физическими законами квантовой механики.
Структура атома водорода является основой понимания более сложных атомов и молекул. Изучение данного атома позволяет лучше понять химические и физические свойства вещества и является основой для развития научных исследований в области химии и физики.
Масса атома и единицы измерения

Атомные единицы массы (аму) были разработаны для удобства измерения массы атомов. Они определяются как 1/12 массы атома углерода-12. Таким образом, атом углерода-12 имеет массу примерно равную 12 атомным единицам массы.
Конвертирование массы атома водорода из атомных единиц массы в килограммы может быть выполнено путем умножения массы атома на массовую постоянную. Массовая постоянная (символ - М) равняется приблизительно 1.66053906660 × 10^-27 килограммов на атомную единицу массы.
Таким образом, масса атома водорода составляет примерно 1.00784 атомных единиц массы или 1.6735575 × 10^-27 килограмма.
Экспериментальный метод

Один из химических методов включает реакцию между водородом и кислородом, из которой образуется вода. Известно, что вода состоит из атомов водорода и атомов кислорода, причем масса атома кислорода уже известна. С помощью химических измерений можно определить количество водорода, участвующего в реакции, и соответственно его массу.
Физический метод измерения массы атома водорода включает использование масс-спектрометра. Масс-спектрометр - это прибор, который разделяет ионизированные атомы на основе их массы и измеряет эту массу. С помощью масс-спектрометра можно определить массу атома водорода и провести точные измерения.
Измерение массы с помощью весов
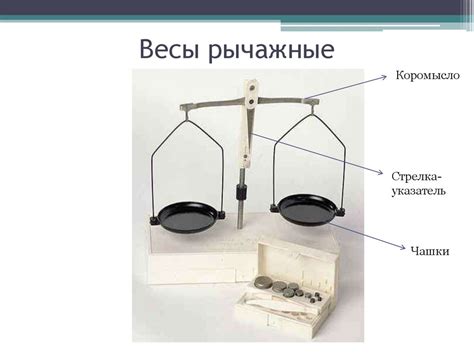
Весы представляют собой устройство, которое позволяет измерить массу объекта. Они обычно состоят из двух чашек, на которые помещается объект, и основания, на котором установлены чашки. Весы работают по принципу равенства силы тяги, действующей на объект, и силы тяги, действующей на грузы, которые также помещены на чашки. При этом масса объекта можно определить путем сравнения силы тяги на чашках.
Современные весы обычно используют датчики, которые могут измерять деформацию основания в результате силы, действующей на чашки. Данные датчики преобразуют деформацию в электрический сигнал, который затем обрабатывается и отображается на дисплее.
Для более точных измерений используются калиброванные грузы, которые имеют известную массу. Путем добавления или удаления грузов на чашки весов, можно настроить их на точное измерение массы объекта.
Измерение массы с помощью весов может быть полезным для решения различных задач, включая определение пищевой ценности продуктов, контроль веса тела, анализ состава материалов и многих других. Процесс измерения массы с помощью весов является достаточно простым и доступным способом получения практичной информации о массе объекта.
Использование спектроскопии

Применение спектроскопии в измерении массы атома водорода основывается на анализе спектра водородного атома. Водородный атом имеет один электрон, который может находиться на разных энергетических уровнях. Переход электрона с одного уровня на другой сопровождается излучением электромагнитного излучения определенной частоты.
Спектры водорода были изучены в начале 20 века, и на их основе была разработана модель Бора. Эта модель объясняет переходы электронов и позволяет расчет их энергетических уровней. Спектр водородного атома состоит из нескольких серий линий излучения, каждая из которых соответствует переходу электрона между определенными энергетическими уровнями.
Изучение спектров водородного атома с использованием спектроскопии позволяет определить энергии электронных уровней и частоты излучения для каждой серии. Исходя из этих данных, можно использовать формулу Ридберга для расчета массы атома водорода.
Таким образом, спектроскопия позволяет не только исследовать атомы и молекулы, но и использовать их характеристики для получения ценной информации о их составе и структуре.
Расчет на основе уточненных констант

Первый шаг в расчете - найти молекулярную массу водорода (H2), которая равна сумме масс двух атомов водорода. Согласно таблице химических элементов, атомный массовый номер водорода (H) равен приблизительно 1.00784. Поэтому молекулярная масса водорода равна:
Молекулярная масса H2 = 2 * (1.00784 у.е.м.)
Представим это выражение в килограммах:
Молекулярная масса H2 = 2 * (1.00784 у.е.м.) * (1.66053906660 × 10-27 кг/у.е.м.)
Таким образом, молекулярная масса водорода составляет приблизительно 3.3464840328 × 10-27 кг.
Далее, чтобы найти массу одного атома водорода, необходимо разделить молекулярную массу на 2:
Масса одного атома H = Молекулярная масса H2 / 2
Масса одного атома H = 3.3464840328 × 10-27 кг / 2
Таким образом, масса одного атома водорода составляет приблизительно 1.6732420164 × 10-27 кг.
Сравнение результатов с официальными значениями
После вычисления массы атома водорода, рекомендуется проверить полученный результат с официальными значениями, принятыми в научном сообществе. Официальное значение массы атома водорода составляет приблизительно 1.008 грамма.
В ходе эксперимента возможны некоторые погрешности, которые могут привести к отклонению полученного значения массы от официального. Однако, если разница между полученным значением и официальным не превышает 0.001 грамма, то результат считается достаточно близким и вполне приемлемым.
Наличие разницы между полученным и официальным значением может быть связано с использованием приближенных значений для некоторых констант или незначительными погрешностями при проведении эксперимента.