Таблица Менделеева - это уникальный инструмент, который помогает нам разобраться во всем многообразии элементов, составляющих наш мир. В ней содержатся не только данные о символах и атомных номерах элементов, но и другая полезная информация, включая число протонов и электронов в атоме.
Однако, каждый атом также содержит определенное число нейтронов, которые оказывают влияние на его свойства и химическую активность. Но как найти это число нейтронов по таблице Менделеева? Все очень просто!
Чтобы найти число нейтронов атома, нужно знать его атомный номер и атомную массу. Обычно эти данные указаны в таблице Менделеева. Атомный номер представляет собой количество протонов в ядре атома. Атомная масса - это средняя масса атомов данного элемента, которая учитывает количество протонов и нейтронов в атоме.
Чтобы найти число нейтронов, нужно от атомной массы отнять атомный номер. Полученное число будет равно числу нейтронов в атоме данного элемента. Например, для кислорода атомный номер равен 8, а атомная масса - примерно 16. Подставив эти значения в формулу, получим, что кислород содержит примерно 8 нейтронов.
Появление теории атома
Понятие атома появилось в древнегреческой философии и было предложено в качестве объяснения структуры и разнообразия мира. Однако, только в 19 веке появилась научная теория атома, основанная на экспериментах и математических моделях.
Одним из основоположников современной атомной теории является Джон Дальтон, который в 1804 году сформулировал основные положения атомной теории. Согласно его модели, атомы представляют собой неделимые и неделимые частицы, из которых строится вся материя. Атомы различных элементов имеют разные свойства и сочетаются между собой при химических реакциях в определенных пропорциях.
Для уточнения структуры атомов были проведены различные эксперименты, включая опыты по рассеянию частиц, проведенные Эрнестом Резерфордом в 1911 году. Результаты этих экспериментов позволили развить модель атома, согласно которой атом состоит из положительно заряженного ядра и электронов, движущихся вокруг него по орбитам.
Современная модель атома дополняется теорией квантового механизма, которая описывает поведение частиц на очень маленьких расстояниях. Поэтому с помощью таблицы Менделеева можно найти число нейтронов атома, зная его атомный номер и массовое число.
| Элемент | Атомный номер | Массовое число | Число нейтронов |
|---|---|---|---|
| Водород | 1 | 1 | 0 |
| Углерод | 6 | 12 | 6 |
| Кислород | 8 | 16 | 8 |
| Железо | 26 | 56 | 30 |
Исторические сведения

Таблица Менделеева, разработанная русским химиком Дмитрием Менделеевым в 1869 году, стала важным инструментом организации химических элементов и предсказания отсутствующих элементов.
Создание таблицы Менделеева помогло установить систематическую связь между различными химическими элементами и распределить их по порядку возрастания атомного номера. Важным достоинством таблицы является ее способность предсказывать свойства отсутствующих на момент разработки элементов. Благодаря таблице Менделеева были открыты новые элементы, подтверждающие правильность его системы.
Сегодня таблица Менделеева признается всемирным наследием и основным инструментом химиков по всему миру. Она позволяет исследователям понять и классифицировать свойства химических элементов, а также помогает предсказывать и изучать новые элементы и их соединения.
Современные представления о структуре атома
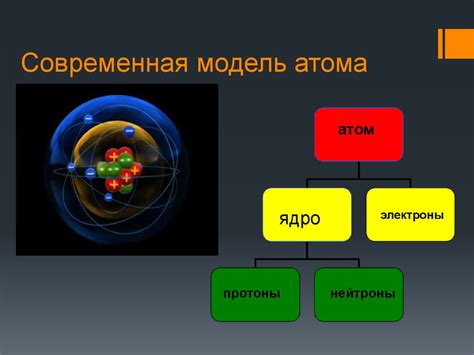
Согласно этой модели, атом состоит из ядра, которое содержит протоны и нейтроны, и электронов, движущихся вокруг ядра на определенных энергетических уровнях - электронных оболочках. Протоны имеют положительный заряд, нейтроны не обладают зарядом, а электроны имеют отрицательный заряд.
Протоны и нейтроны находятся в ядре атома, которое занимает очень маленький объем, по сравнению с общим объемом атома. Оболочки с электронами располагаются вокруг ядра и занимают главным образом объем атома.
Число протонов в ядре определяет атомный номер элемента и является постоянным для данного элемента. Число нейтронов в атоме может варьироваться и называется нуклонным числом. Число нуклонов в атоме, включая протоны и нейтроны, называется атомным массовым числом.
Все элементы периодической системы Менделеева упорядочены по возрастанию атомного номера, что позволяет нам определить количество протонов в атоме элемента, а, следовательно, его атомный номер. Чтобы найти число нейтронов атома, нужно вычесть атомный номер из атомного массового числа.
Нейтроны и их роль в атоме

Главная роль нейтронов в атоме заключается в их способности поддерживать стабильность ядра. Нейтроны, находящиеся в ядре, обуславливают его массу и являются "склеивающим клеем" для протонов, так как они способны преодолевать отталкивающее взаимодействие протонов и удерживать их вместе в ядре.
Количество нейтронов в атоме может варьироваться. Это значение называется нуклонным числом и обозначается символом N. Чтобы найти число нейтронов в атоме по таблице Менделеева, нужно знать атомный номер элемента, обозначаемый символом Z. Формула для определения числа нейтронов выглядит следующим образом: N = A - Z, где A – это атомная масса элемента, которая указана в таблице Менделеева.
Нейтроны играют важную роль в ядерных реакциях и различных технологиях, так как могут быть использованы для управления делением и слиянием ядер, что приводит к выделению энергии. Изучение нейтронов помогает ученым лучше понять строение и свойства атомов, а также применять этот знания в различных областях науки и техники.
Что такое нейтроны?
Нейтроны имеют массу почти равную массе протонов, поэтому их суммарная масса в ядре определяет атомную массу элемента. Именно количество нейтронов в ядре атома определяет его изотоп и его свойства.
Нейтроны также играют важную роль в ядерных реакциях. Они могут быть выбиты из ядра атома путем столкновений с другими частицами или поглощены ядром, превращая его в другой элемент. Кроме того, нейтроны используются в ядерной энергетике, в науке и в других сферах для проведения экспериментов и исследований.
Методы определения числа нейтронов атома

Число нейтронов в атоме можно определить не только по таблице Менделеева, но и с помощью различных методов изучения атомных свойств. Некоторые из них включают:
| Метод | Описание |
|---|---|
| Масс-спектрометрия | Этот метод основан на разделении атомов по их отношению массы к заряду. Путем анализа масс-спектра можно определить отношение массы атома к его заряду и, следовательно, число нейтронов в атоме. |
| Ядерная магнитная резонансная спектроскопия (ЯМР) | ЯМР спектроскопия использует взаимодействие магнитных моментов ядер с электромагнитным излучением для определения числа нейтронов в атоме. Путем анализа ЯМР спектра можно получить информацию о спиновых состояниях ядер, из которых можно вычислить число нейтронов. |
| Рентгеноструктурный анализ | Этот метод использует рентгеновское излучение, проходящее через кристалл, чтобы получить информацию о расположении атомов в структуре. Путем анализа рентгеноструктурной дифракции можно определить расстояния между атомами, что помогает в определении числа нейтронов. |
Это только некоторые из методов, которые используются для определения числа нейтронов в атоме. Каждый из них имеет свои преимущества и ограничения, и выбор метода зависит от конкретной ситуации и целей исследования.