Химия – это удивительная наука, которая исследует строение и свойства различных веществ. А одной из основных составляющих многих веществ являются соли. Соли в химии – это соединения, в которых катионы металла или аммония соединены с анионами, которые обычно являются кислотными остатками. Как определить соль по формуле и какие методы использовать для этого?
При определении соли по формуле необходимо знать, какие ионы есть в ее составе. Самый простой и надежный способ определить соль – это посмотреть на ее структурную формулу. В структурной формуле соли первым символом указывается катион, а вторым – анион. Например, формула NaCl сообщает нам, что соль содержит натрий (Na+) и хлор (Cl-). Таким образом, определение основных ионов соли является первым шагом для определения соли по формуле.
Кроме того, каждый ион может иметь различные степени окисления, что делает процесс определения соли более сложным. Чтобы определить соль по формуле с ионами различной степени окисления, необходимо учитывать заряд каждого иона. Для этого можно использовать таблицу степеней окисления элементов в соединениях или обратиться к справочной литературе. Например, формула FeCl3 указывает на ионы железа (+3) и хлора (-1). Таким образом, определение зарядов ионов является следующим важным шагом в процессе определения соли по формуле.
Определение соли в химии по формуле: методы и примеры
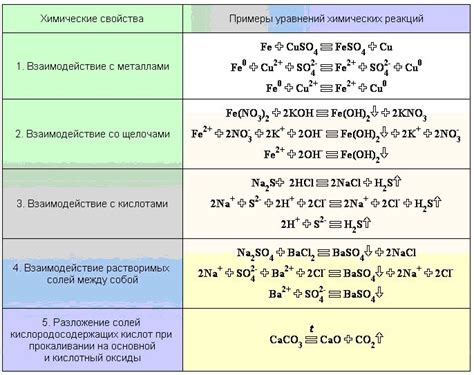
Существует несколько методов, которые помогают определить соль по ее формуле. Один из таких методов включает анализ строения и состава ионов, входящих в соединение. Каждый ион имеет свои уникальные свойства, которые позволяют определить, с какими другими ионами он может образовывать соль. Например, соль NaCl состоит из иона натрия (Na+) и иона хлора (Cl-).
Другой метод определения соли по формуле - это расчет молекулярной массы соединения. Зная массу каждого элемента в соли и их количество, можно вычислить общую массу соли. Например, молярная масса соли NaCl равна сумме массы атома натрия и массы атома хлора.
Пример:
Дана формула соли H2SO4. Чтобы определить эту соль, нужно проанализировать состав ионов. Из формулы видно, что она состоит из иона водорода (H+) и ионов серы (SO4^2-). Таким образом, это сульфатная соль серы.
Также, можно произвести расчет молекулярной массы. С учетом атомных масс каждого элемента (водорода, серы и кислорода) и их количества в формуле соли, можно вычислить массу соли H2SO4.
Таким образом, определение соли в химии по формуле включает анализ состава ионов и расчет молекулярной массы соединения. Эти методы помогают идентифицировать и классифицировать соль в рамках химической номенклатуры.
Методы определения соли в химии
Соли в химии можно определить с помощью различных методов, основанных на химических реакциях и особенностях состава соли.
Один из методов определения соли - метод анализа отложений. При этом методе соль обрабатывается растворителем, а получившееся растворение затем анализируется с помощью различных химических реакций.
Еще одним методом определения соли является метод термического анализа. При этом методе соль подвергается нагреванию и процесс изменения ее массы и химических свойств изучается.
Важно отметить, что для определения соли в химии часто используются комбинации различных методов, чтобы получить более точные и достоверные результаты.
Анализ химической формулы соли
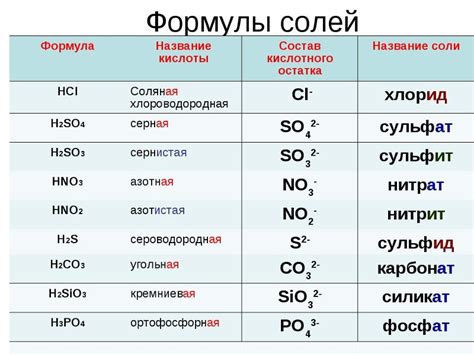
Химическая формула соли состоит из двух частей: катиона и аниона. Анализ химической формулы соли позволяет определить состав и свойства соли.
Сначала необходимо определить катион, который является положительно заряженной частицей соли. Катионы обычно являются металлами или положительно заряженными радикалами. Для определения катиона необходимо внимательно рассмотреть формулу соли. Например, в формуле NaCl катионом является Na (натрий), а в формуле CaCO3 катионом является Ca (кальций).
Затем необходимо определить анион, который является отрицательно заряженной частицей соли. Анионы обычно являются неметаллами или отрицательно заряженными радикалами. Для определения аниона необходимо также внимательно рассмотреть формулу соли. Например, в формуле NaCl анионом является Cl (хлор), а в формуле CaCO3 анионом является CO3 (карбонат).
Определение состава соли по химической формуле позволяет понять, какие элементы и соединения входят в состав соли, а также предсказать ее свойства и способы применения. Анализ химической формулы соли играет важную роль в химических исследованиях, а также в промышленности и медицине.
Использование химических реакций для определения соли
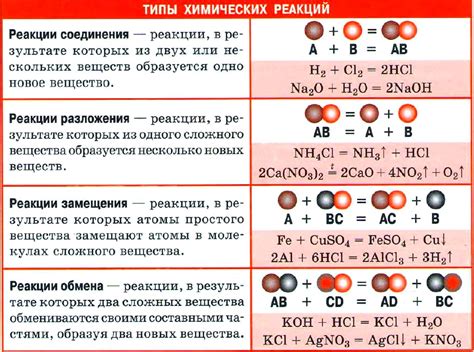
Химические реакции могут быть полезным инструментом для определения наличия и состава солей. При соединении с другими химическими веществами соли могут проявить свои уникальные свойства, что делает возможным их идентификацию.
Один из наиболее распространенных методов определения солей - образование осадка. Когда смешивают растворы соли с растворами других реагентов, может возникнуть неликвидный осадок в результате образования новых соединений. Этот осадок может быть точным индикатором наличия и типа соли.
Другой метод - использует свойства солей, чтобы вызвать цветовую реакцию. Некоторые соли при взаимодействии с определенными реагентами изменяют свой цвет. Например, реакция между соляной кислотой и хлоридом бария приводит к образованию белого осадка, что указывает на наличие бария в исходной соли.
Также используется метод нагревания соли. Когда соль подвергается нагреванию до определенной температуры, она может деградировать и изменять свою структуру или цвет. Это изменение может помочь определить тип соли.
Определение солей с использованием химических реакций требует достаточной химической экспертизы, чтобы правильно идентифицировать и интерпретировать полученные результаты. Поэтому рекомендуется проводить такие определения только под руководством профессионала или в специализированной химической лаборатории.
Примеры определения соли в химии
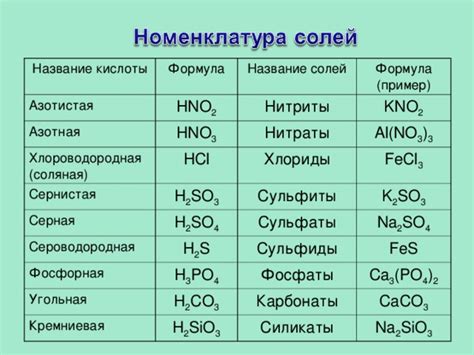
Соли могут быть определены в химии с использованием различных методов и реакций. Вот несколько примеров:
Метод анализа раствора соли. Для этого раствор соли смешивается с веществом, способным выделять их осадок. Например, если к раствору хлорида натрия добавить немного серной кислоты, образуется осадок серного аниона (SO42-).
Метод анализа ионов в соли. Этот метод основан на том, что различные ионы при добавлении определенных реактивов образуют уникальные осадки или цветные соединения. Например, добавление немного аммиачного раствора к раствору солей меди (Cu2+) вызывает образование голубого осадка гидроксида меди (Cu(OH)2).
Использование специальных реактивов для определения солей. Например, карбонат иона, присутствующий в некоторых солях, может быть определен с помощью добавления кислоты и наблюдения за выделением пузырьков газа (CO2) и путилков аммиачной кислоты.
Это лишь несколько примеров методов определения солей в химии. В зависимости от конкретной соли и требуемого результата, могут применяться и другие методы и реакции.
Спектральный анализ солей
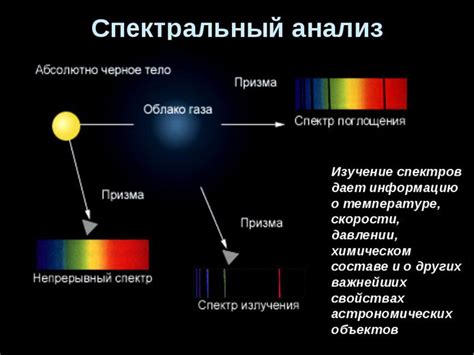
Для проведения спектрального анализа солей используются специальные устройства - спектрофотометры. Они позволяют измерять интенсивность света в зависимости от его длины волны, что позволяет определить конкретные элементы, присутствующие в рассматриваемой соли.
Спектры поглощения и излучения солей включают в себя серию характерных линий, которые соответствуют различным энергетическим переходам внутри атомов или молекул. Частота и интенсивность этих линий позволяют определить наличие конкретного элемента в соли.
Примером спектрального анализа солей может служить определение содержания железа в сульфате железа(II) (FeSO4). При проведении спектрального анализа этой соли будет видно характерные линии, соответствующие железу.
Таким образом, спектральный анализ является мощным инструментом для определения солей в химии, позволяющим достоверно идентифицировать присутствующие вещества на основе их спектральных характеристик.
Использование химического анализа для определения соли

Качественный анализ солей основан на определении присутствия или отсутствия определенных ионов в растворе. Для этого используются различные реактивы, которые образуют характерные осадки или окрашивают растворы в определенные цвета.
Например, для определения хлорида, можно использовать азотную кислоту и серебро нитрат. При реакции хлорида с серебро нитратом образуется белый осадок серебряного хлорида AgCl.
| Соль | Реактив | Результат |
|---|---|---|
| Хлорид | Серебро нитрат | Белый осадок AgCl |
Количественный анализ позволяет определить концентрацию соли в растворе. Для этого используются различные методы, такие как гравиметрический, волюметрический, а также инструментальные методы, включающие использование спектрофотометрии, электрометрии и др.
Например, для определения концентрации хлорида в растворе можно использовать волюметрический метод, основанный на реакции осаждения хлорида с серебро нитратом. При добавлении избытка серебро нитрата и использовании индикатора, можно определить точный объем реактива, необходимый для полного осаждения всех ионов хлорида.
Таким образом, химический анализ является важным инструментом для определения солей. Он позволяет провести не только качественное, но и количественное определение соли, что является основой для многих исследований и практического применения в химической промышленности.