Валентность - это важное понятие в химии, которое помогает понять, какие ионы, атомы или группы атомов могут образовывать химические соединения. В простых терминах валентность - это "способность" атома объединяться с другими атомами. Знание валентности позволяет нам предсказывать и объяснять свойства и реакции различных соединений.
Для определения валентности атома нужно взглянуть на его электронную конфигурацию, то есть расположение и количество электронов в его электронных оболочках. Валентность атома будет соответствовать числу электронов, которые он может отдать или принять при образовании химических связей.
Чтобы проиллюстрировать это, рассмотрим пример с натрием (Na) и хлором (Cl). Натрий имеет атомную структуру 2-8-1, то есть у него 11 электронов. Он имеет один электрон в своей внешней электронной оболочке, которую называют "n-оболочкой". Хлор имеет структуру 2-8-7, то есть у него 17 электронов. Он нуждается в одном электроне, чтобы заполнить свою n-оболочку.
Определение понятия "валентность" в химии
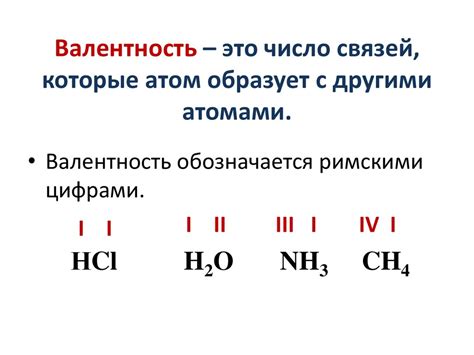
Валентность обычно обозначается римскими цифрами, и она может быть положительной или отрицательной, в зависимости от того, должен ли атом отдать или получить электроны. Если атом образует положительные ионы, валентность будет равна числу электронов, которые атом может отдать другому атому. Если атом образует отрицательные ионы, валентность будет равна числу электронов, которые атом может получить от другого атома.
Знание валентности элементов позволяет прогнозировать их химические свойства и способность образовывать соединения. Валентность также играет важную роль при написании химических формул и уравнений реакций.
Например, хлор (Cl) имеет валентность -1, так как он может получить один электрон от другого атома, чтобы образовать отрицательный ион. Алюминий (Al) имеет валентность +3, так как он может отдать три электрона другому атому, чтобы образовать положительный ион.
Значение валентности для химических реакций
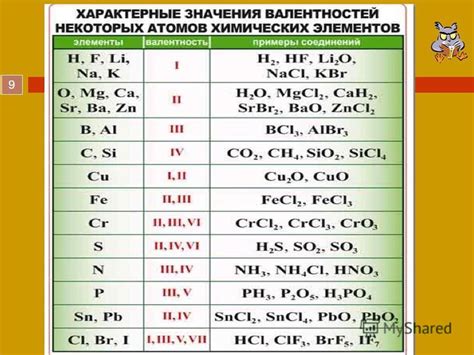
Валентность определяется по количеству электронов во внешней электронной оболочке атома. Валентные электроны могут быть переданы от одного атома к другому или образовать общую электронную пару. Это влияет на образование химических связей и определяет типы реакций, которые могут происходить между различными элементами.
Зная валентность различных элементов, можно предсказать, сколько атомов одного элемента нужно для образования химического соединения с атомами другого элемента. Например, если у элемента А валентность 2, а у элемента В - 1, то для образования стабильного химического соединения между ними потребуется 2 атома В на каждый атом А.
Значение валентности также позволяет определить степень окисления атома в химическом соединении. Окислительные и восстановительные реакции основаны на изменении степени окисления атомов. Степень окисления атома вещества зависит от его валентности.
Важно понимать, что валентность может быть переменной и зависеть от конкретных условий и окружающих атомов. Она также может быть представлена в виде положительного или отрицательного числа, что указывает, что атом принимает или отдает электроны соответственно.
Валентность играет ключевую роль в понимании и изучении химических реакций. Она позволяет установить соотношение между различными элементами и предсказать их поведение при реакциях. Поэтому знание валентности является важным для понимания основ химии и проведении химических экспериментов.
Как определить валентность элемента
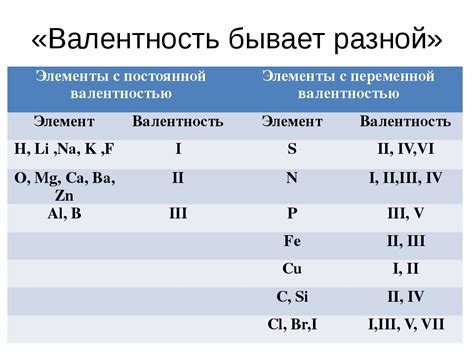
Валентность элемента определяется на основе его электронной конфигурации и числа валентных электронов. Валентность указывает на количество электронов, которые элемент готов отдать или принять при образовании химических связей.
Существуют несколько способов определения валентности элемента:
- Таблица Менделеева: Большинство химических элементов имеет постоянную валентность, которую можно узнать из таблицы Менделеева. Валентность указывается в верхней части клетки элемента. Например, у кислорода (О) валентность равна 2.
- Электронная конфигурация: Электронная конфигурация элемента показывает распределение его электронов по энергетическим уровням и подуровням. Последний заполненный энергетический уровень и число электронов на нем определяют валентность элемента. Например, у натрия (Na) последний заполненный энергетический уровень имеет 3s^1 конфигурацию, поэтому валентность Na равна 1.
- Число валентных электронов: Валентность элемента также можно определить по числу валентных электронов, которые находятся на его последнем энергетическом уровне. Например, у кальция (Ca) последний заполненный энергетический уровень имеет 4s^2 конфигурацию, значит, валентность Ca равна 2.
Определение валентности элемента имеет важное значение при составлении химических формул, предсказании химических реакций и понимании химических свойств веществ.
Практические примеры определения валентности

Существует несколько способов определения валентности элементов. Один из них - анализ химических формул веществ. Например, водород (H) образует соединение с кислородом (O), известное как вода (H2O). Химическая формула показывает, что водороду необходимо отдать два электрона, чтобы образовать химическую связь с кислородом. Следовательно, валентность водорода равна 1.
Другой пример - молекула хлорида натрия (NaCl). Хорлоид натрия состоит из ионов натрия (Na+) и хлора (Cl-). Натрий отдает один электрон, а хлор принимает его. Таким образом, валентность натрия равна 1, а валентность хлора равна 1.
Третий пример - кислород (O) образует соединение с азотом (N) и водородом (H), известное как аммиак (NH3). Молекула аммиака состоит из азота и трех атомов водорода. Азот принимает три электрона от трех атомов водорода, поэтому его валентность равна 3. Атомы водорода каждый отдают один электрон, поэтому их валентность равна 1.
Таким образом, практическое определение валентности элементов позволяет лучше понять химические свойства и реакции веществ.
Как найти валентность в химии 8 класс
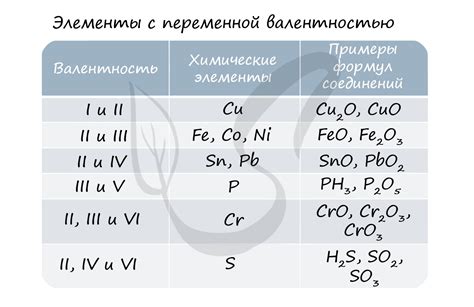
Валентность элемента в химии определяет, сколько валентных электронов имеет атом этого элемента. Зная валентность элемента, можно предсказать его химические свойства.
Существует несколько способов определения валентности элемента:
| Способ | Описание |
|---|---|
| 1. По номеру группы | Валентность элемента можно определить по номеру группы, в которой он находится в таблице Менделеева. Например, элементы группы 1 имеют валентность 1, элементы группы 2 - валентность 2, а элементы группы 17 - валентность 7. |
| 2. По электронной конфигурации | Валентность элемента можно определить по его электронной конфигурации. Для этого надо посмотреть на количество электронов во внешней оболочке атома. Например, атомы с одним-двумя электронами во внешней оболочке имеют валентность 1-2, а атомы с семью электронами - валентность 7. |
| 3. По формуле химического соединения | Валентность элемента можно определить по формуле химического соединения. Например, водород (H) обычно имеет валентность 1, аллюминий (Al) - валентность 3, а кислород (O) - валентность 2. Исходя из этого, по формуле воды (H2O) можно определить валентность кислорода - 2. |
Зная валентность элемента, можно определить его способность связываться с другими элементами и составлять химические соединения. Пользуйтесь представленными способами определения валентности, чтобы лучше понимать строение и свойства элементов.
Особенности определения валентности восьмиклассниками

Одной из особенностей определения валентности учениками восьмого класса является необходимость понимания основных понятий в химии, таких как атом, ион, валентные электроны и электронная оболочка. Ученики должны понимать, что валентность обусловлена числом валентных электронов во внешней оболочке атома.
Для наглядности и лучшего понимания учениками можно использовать таблицу Менделеева. В таблице Менделеева элементы расположены по возрастанию атомной массы и группами, что позволяет наглядно видеть связь между атомами одной группы и их валентностью. Например, элементы группы 1 имеют одну валентную электронную оболочку и валентность равна 1, а элементы группы 2 имеют две валентные электронные оболочки и валентность равна 2.
Для практического определения валентности ученики могут использовать простые методы, такие как метод карточек. Ученикам следует записать символы элементов на карточки и поставить соответствующее количество значков, отражающих количество валентных электронов. Затем ученики могут соединить карточки таким образом, чтобы количество значков на каждой карточке соответствовало валентности элементов, образующих соединение.
Важным аспектом для практического определения валентности является проведение экспериментов с химическими соединениями. Ученикам можно предложить провести эксперименты с различными элементами, соединениями и реакциями, чтобы наблюдать изменение валентности в процессе образования химических соединений.
| Элемент | Валентность |
|---|---|
| Водород | 1 |
| Кислород | 2 |
| Натрий | 1 |
| Железо | 2, 3 |
| Сера | 2, 4, 6 |
Важность практического руководства по определению валентности

Практическое руководство по определению валентности имеет большую важность в обучении химии. Оно позволяет ученикам получить опыт практического применения теоретических знаний и развить навыки лабораторной работы.
Практическое руководство позволяет ученикам не только запомнить теоретические сведения, но и усвоить их на практике. Оно помогает учащимся стать активными участниками в своем обучении и развивает их критическое мышление.
Советы по использованию практического руководства

Практическое руководство по поиску валентности в химии предназначено для учащихся 8 класса. Вот несколько советов, которые помогут вам максимально эффективно использовать данное руководство:
Внимательно прочитайте введение и общую информацию о понятии валентности. Понимание основных принципов и определений поможет вам успешно использовать дальнейшие методы и инструкции.
Изучите примеры из руководства и попробуйте решить задачи самостоятельно. Постепенно повторяйте и закрепляйте материал, чтобы улучшить свои навыки в определении валентности.
Пользуйтесь шаблонами и таблицами, предоставленными в руководстве. Они помогут вам систематизировать информацию и упростить процесс определения валентности.
Если у вас возникнут вопросы, не стесняйтесь обратиться к своему учителю химии. Он сможет разъяснить непонятные моменты и дать дополнительные объяснения.
Практикуйтесь на дополнительных задачах и упражнениях, которые также могут быть указаны в руководстве. Чем больше практики, тем лучше вы будете понимать и применять материал.
Не бойтесь экспериментировать и пробовать различные методы определения валентности. Иногда только практика может научить вас лучшему подходу к решению задач.
Соблюдение этих советов поможет вам эффективно использовать практическое руководство и лучше понять понятие валентности в химии. Удачи в изучении!
| Метод | Примеры применения |
|---|---|
| Анализ электронной структуры | Na - валентность 1, Cl - валентность 1 |
| Анализ оксионов | SO42- - валентность 6 |
| Анализ радикалов | OH - валентность 1, CO32- - валентность 2 |