Масса атома – одно из основных понятий в физике и химии. Это величина, которая определяет массу отдельного атома элемента. Но как же ее найти? Как вычислить массу атома? Процесс не так прост, как может показаться на первый взгляд. Тем не менее, существует надежная и проверенная формула для расчета массы атома.
Атом является основным строительным блоком вещества и состоит из ядра и электронной оболочки. Ядро состоит из нейтронов и протонов, а электронная оболочка содержит электроны. Если мы узнаем массу нейтрона, протона и электрона, то сможем рассчитать массу отдельного атома.
Формула для нахождения массы атома выглядит следующим образом: масса атома = количество нейтронов × масса нейтрона + количество протонов × масса протона + количество электронов × масса электрона. Полученное значение массы атома измеряется в атомных единицах массы (a.m.u.) или десятых долях массного числа (u).
Что такое масса атома? Определение и единицы измерения

Единицей измерения массы атома является атомная единица массы (а.е.м). Она равна 1/12 массы атома углерода-12. Так как масса атома углерода-12 составляет приблизительно 1,992646 × 10^-26 килограмма, то атомная единица массы равна примерно 1,660539 × 10^-27 килограмма.
Помимо атомной единицы массы, для измерения массы атомов в физике также используется дециграмм (дг) и грамм (г). Один дециграмм равен 10^-1 грамму, а один грамм равен 10^-3 килограмма.
Зная массу атома, можно проводить различные расчеты и измерения, связанные с веществами и их взаимодействием. Масса атома является одним из ключевых параметров в физике и химии, позволяющих изучать структуру и свойства различных веществ и материалов.
Формула расчета массы атома

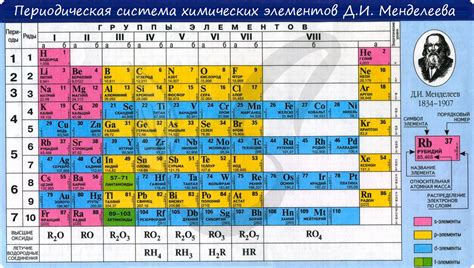
- Определите атомный номер элемента (Z). Он указывает на порядковый номер элемента в периодической системе Менделеева.
- Найдите массовое число (A) элемента. Оно указывает на общее количество протонов и нейтронов в атоме данного элемента.
- Определите массу протона и нейтрона. Их значения равны примерно 1,6726 × 10-27 кг.
- Рассчитайте массу атома по формуле: Масса атома = (масса протона × количество протонов) + (масса нейтрона × количество нейтронов).
Например, давайте рассчитаем массу атома углерода (C):
- Атомный номер углерода равен 6.
- Массовое число углерода равно 12.
- Масса протона и нейтрона составляет приблизительно 1,6726 × 10-27 кг.
- Рассчитаем массу: Масса атома углерода = (1,6726 × 10-27 кг × 6) + (1,6726 × 10-27 кг × 6) = 3,3452 × 10-26 кг.
Таким образом, масса атома углерода составляет примерно 3,3452 × 10-26 кг.
Примеры расчетов массы атома различных элементов
Масса атома кислорода (O):
В атомном весе кислорода A=16 г/моль. По определению, одна моль атомов кислорода содержит N=6.02214076x10^23 атомов. Для расчета массы одного атома кислорода можно использовать формулу: масса атома = A/N.
Масса атома кислорода = 16 г/моль / (6.02214076x10^23 атомов) ≈ 2.66x10^-23 г.
Масса атома железа (Fe):
Атомный вес железа A=55.845 г/моль. Количество атомов в одной моли железа N=6.02214076x10^23 атомов. Масса атома железа может быть рассчитана по формуле: масса атома = A/N.
Масса атома железа = 55.845 г/моль / (6.02214076x10^23 атомов) ≈ 9.27x10^-23 г.
Масса атома алюминия (Al):
Атомный вес алюминия A=26.982 г/моль. Количество атомов в моли алюминия N=6.02214076x10^23 атомов. Масса атома алюминия можно вычислить по формуле: масса атома = A/N.
Масса атома алюминия = 26.982 г/моль / (6.02214076x10^23 атомов) ≈ 4.49x10^-23 г.
Расчеты массы атома представлены выше только в качестве примера. Для других элементов можно использовать аналогичные расчеты, заменяя значения атомного веса соответствующими значениями для данного элемента.