Кислотное оксидирование - процесс, в результате которого происходит образование веществ, содержащих кислород, при реакции различных веществ с кислородом, поступающим из воздуха. Кислотные оксиды имеют сильно выраженные кислотные свойства и активно реагируют с водой.
Определение кислотности оксида проводится с использованием различных методов и реактивов. Одним из наиболее распространенных способов является метод титрования. При данном методе раствор оксида, который содержит искомый оксид, помещают в колбу, затем добавляют измеренное количество вещества, идущего в реакцию с оксидом. Постепенно добавляют титрующий раствор, пока не достигнется полное окисление оксида. В результате подсчитывается точное количество титрующего раствора, которое необходимо для достижения точки эквивалентности.
Кислотные оксиды обладают широким спектром применения в различных отраслях промышленности. Они широко используются в химической промышленности для производства различных кислот, солей и других химических соединений. Кроме того, некоторые кислотные оксиды, такие как оксид серы, оксид азота и оксид углерода, являются значимыми загрязняющими веществами, отбрасываемыми в атмосферу промышленными предприятиями. В основном, их согласно стандартам качества воздуха слудует минимизировать или полностью устранить, так как они являются одними из основных виновников загрязнения окружающей среды.
Что такое кислотность оксида?

Когда оксиды растворяются в воде, молекулы воды реагируют с атомами кислорода, образуя гидроксиды или кислоты. Если оксид образует кислоту при реакции с водой, такой оксид считается кислотным. Кислотность оксида зависит от активности атома, от которого он образован. Активность атома, в свою очередь, зависит от электроотрицательности этого атома.
Кислотность оксидов можно определить с помощью специальных методов, таких как потенциометрический титр, качественные реакции и гравиметрический метод. Анализ кислотности оксидов важен в химической промышленности и научных исследованиях, так как позволяет оценить их свойства и потенциальное применение в различных областях.
| Тип оксида | Кислотность оксида |
|---|---|
| Кислый | Образует кислоты при реакции с водой |
| Щелочной | Образует щелочи при реакции с водой |
| Нейтральный | Не образует ни кислоты, ни щелочи при реакции с водой |
Изучение кислотности оксидов позволяет понять их реакционную способность и использовать их в различных отраслях химии, таких как синтез органических соединений, производство удобрений и лекарственных препаратов, а также в промышленности стекла, металлургии и электроники.
Основные понятия кислотности оксида

Для определения кислотности оксидов применяются различные методы, включая:
- Индикаторные методы: основаны на использовании индикаторов, которые меняют цвет при контакте с кислотами или щелочами. Например, универсальный индикатор изменяет цвет в зависимости от pH окружающей среды.
- Физико-химические методы: включают измерение pH с помощью pH-метра или использование электродов, которые регистрируют изменение потенциала.
- Количественные методы: позволяют определить точное значение pH окружающей среды с использованием различных реактивов и приборов.
Определение кислотности оксидов имеет широкое применение в различных областях, включая химическую промышленность, медицину, экологию и научные исследования. Кислотные оксиды используются в производстве кислот, солей и других химических соединений. Знание кислотности оксидов является важным при разработке новых материалов и веществ, а также в поддержании правильного pH в биологических системах.
Определение кислотности оксида
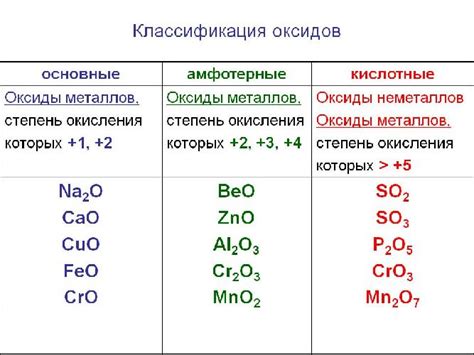
Существует несколько методов для определения кислотности оксида:
- Использование литмусовой бумаги. Литмусовая бумага меняет свой цвет при контакте с кислотными или основными растворами. Если оксид образует кислотный раствор, литмусовая бумага будет красной.
- Использование индикатора pH. Индикаторы pH - это вещества, меняющие свой цвет в зависимости от кислотности или щелочности раствора. Если оксид образует кислотный раствор, индикатор pH будет показывать значение ниже 7.
- Использование нейтрализации с помощью щелочи. Оксид можно нейтрализовать, добавив к нему щелочь и измерив количество щелочи, необходимой для полной нейтрализации. Чем больше щелочи требуется, тем более кислотный оксид.
Знание кислотности оксида важно для определения его химических свойств и возможных применений. Кислотные оксиды могут использоваться в процессе производства кислот, а также в качестве катализаторов в различных химических реакциях.
Методы определения кислотности оксида
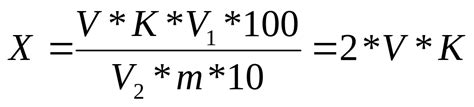
- Количественный анализ - один из основных методов определения кислотности оксида. Он основан на измерении pH-уровня раствора с помощью pH-метра и последующем расчете концентрации кислоты в растворе. Этот метод позволяет получить точные и количественные данные о кислотности оксида.
- Индикаторы - это вещества, которые меняют цвет в зависимости от pH-уровня раствора. Они используются для качественного определения кислотности оксида. Метилоранж (оранжевого цвета при нейтральном pH-уровне) и фенилфталеин (без цвета при нейтральном pH-уровне) - примеры индикаторов, которые широко применяются для определения кислотности оксида.
- Титрование - это метод определения кислотности оксида путем добавления известного объема раствора с известной концентрацией щелочи. В процессе добавления щелочи происходит реакция нейтрализации, и основываясь на объеме и концентрации щелочи, можно определить кислотность оксида.
- Метод кондуктометрии - основан на измерении электропроводности раствора оксида. Кислотные оксиды образуют кислотные растворы, которые обладают большей электропроводностью. Путем измерения электропроводности можно определить кислотность и концентрацию кислотного оксида.
Выбор метода определения кислотности оксида зависит от характеристик оксида, его концентрации и требуемой точности исследования. Комбинация нескольких методов может дать более надежные результаты и позволить получить полное представление о кислотности оксида.
Применение кислотности оксида

Кислотность оксида имеет широкое применение в различных областях науки и промышленности.
1. Металлургия: Кислотность оксидов используется для контроля показателей качества металлов и сплавов. Например, определение кислотности оксида может помочь определить степень окисления материала и его пригодность для дальнейшей обработки и использования.
2. Химическая промышленность: Кислотность оксида может быть использована для контроля и регулирования pH в реакционных смесях в процессе производства различных химических веществ и материалов. Это позволяет оптимизировать процессы синтеза и получить требуемые химические свойства продукта.
3. Очистка воды: Кислотность оксида является одним из показателей качества воды и может использоваться для контроля ее степени загрязненности. Более кислотная вода может требовать дополнительной обработки для удаления вредных примесей и обеспечения безопасности для питья или использования в производственных процессах.
4. Аналитическая химия: Кислотность оксида может быть использована для определения концентрации определенных веществ или соединений в образцах. Это позволяет проводить качественный и количественный анализ различных материалов и определить их состав и свойства.
В итоге, определение и контроль кислотности оксида имеет широкое применение и является важной составной частью многих процессов и исследований в различных отраслях науки и промышленности.
Области применения кислотности оксида

В химии, кислотность оксида помогает определить его реакционную способность и использование в различных химических процессах.
В металлургии, кислотность оксида используется для контроля процессов окисления металлов и создания покрытий на поверхности изделий.
В электронике, кислотность оксида играет роль в процессе нанесения металлических контактов на полупроводниковые материалы.
В экологии, кислотность оксида является важным параметром для анализа загрязнения атмосферы и состояния почвы.
В пищевой промышленности, кислотность оксида используется для регулирования pH-значения пищевых продуктов, что помогает сохранять и улучшать их качество и безопасность.