Fe2O3, или оксид железа(III), является одним из самых распространенных и хорошо известных неорганических соединений. Он обладает ярко выраженными красными оттенками и широко используется в промышленности, медицине и различных технических процессах. Однако, несмотря на свою популярность и широкое применение, Fe2O3 не обладает свойствами реагировать с водой, что лежит в основе рассмотрения данной проблемы.
Реакция между водой и соединением, таким как Fe2O3, может быть описана уравнением химической реакции, в которой соединение разлагается на составляющие его элементы или ионы. Однако Fe2O3 не подвергается такому разложению, не образуя с водой никаких продуктов реакции.
Существует несколько причин, почему Fe2O3 не реагирует с водой. Во-первых, оксиды металлов имеют высокую степень стабильности, что делает их устойчивыми к химическим реакциям. Во-вторых, процесс разложения Fe2O3 на элементы или ионы требует высокой энергии активации, что делает эту реакцию крайне маловероятной при нормальных условиях. И наконец, вода является слабым окислителем, в то время как Fe2O3 имеет окислительные свойства, что также затрудняет возможность их взаимодействия.
Что делает Fe2O3 нереактивным с водой?

Молекула Fe2O3 состоит из двух атомов железа (Fe) и трех атомов кислорода (O), соединенных между собой. Каждый атом железа окружен шестью атомами кислорода, образуя октагональную структуру. В процессе образования этой структуры, электроны в атомах железа распределяются в особых областях, называемых орбиталями. Эта конфигурация электронов делает молекулу Fe2O3 электронейтральной и стабильной.
Вода (H2O), с другой стороны, имеет молекулярную структуру с атомами водорода (H), связанными с атомом кислорода (O). В молекуле воды электроны распределены несколько иначе, что делает ее полярной. Это означает, что молекула воды имеет небольшую разницу в зарядах между атомом кислорода и атомами водорода. Эта полярность влечет к себе другие полярные или заряженные молекулы, что приводит к реакции воды с другими веществами.
В результате отсутствия заряда или полярности в молекуле Fe2O3, она не может взаимодействовать с водой. Поэтому Fe2O3 не реагирует и не растворяется в воде. Однако, если использовать сильные кислоты или щелочи, можно провести процесс растворения Fe2O3.
Стабильность соединения
Эта стабильность объясняется особыми свойствами молекулы Fe2O3. В ее структуре железо связано с кислородом с помощью ковалентных связей, образуя трехмерную кристаллическую решетку.
Эта решетка обладает высокой кристаллической симметрией и формирует прочные связи между атомами железа и кислорода. Это делает соединение Fe2O3 очень стабильным и устойчивым к химическим реакциям.
Кроме того, молекулы Fe2O3 обладают низкой полярностью, что делает их менее склонными к реакциям с полярными растворителями, такими как вода.
В результате, Fe2O3 не проявляет активность при контакте с водой и не растворяется в ней. Это объясняет, почему Fe2O3 не реагирует с водой и остается стабильным соединением.
Структура кристаллической решетки
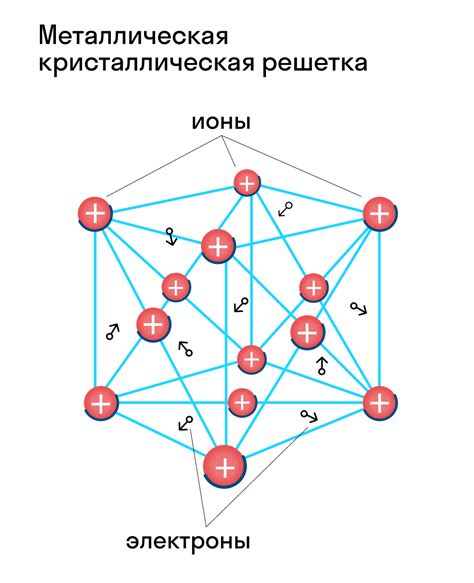
Fe2O3, или трехвалентное железо, образует кристаллическую решетку, которая представляет собой трехмерную упорядоченную сетку железных и кислородных атомов.
В кристаллической структуре Fe2O3, каждый железный атом окружен шестью кислородными атомами, а каждый кислородный атом окружен четырьмя железными атомами. Это образует плотную и устойчивую решетку.
Почему Fe2O3 не реагирует с водой? Вода является кислородсодержащим веществом, но несмотря на присутствие кислорода в молекуле воды, кристаллическая структура Fe2O3 не обладает достаточной реакционной активностью для взаимодействия с водой. Это связано с тем, что взаимодействие между Fe2O3 и водой требует преодоления определенных энергетических барьеров, которые не могут быть преодолены без использования дополнительной энергии.
Таким образом, структура кристаллической решетки Fe2O3 играет важную роль в его химической активности и определяет его способность реагировать с другими веществами, включая воду.
Энергетические условия

Для того чтобы реакция между веществами произошла, необходимо чтобы были выполнены определенные энергетические условия. Рассмотрим почему в данном случае соединение Fe2O3 не реагирует с водой.
Вода является стабильным веществом, однако она может претерпевать химические реакции при наличии активных веществ, которые имеют возможность обеспечить энергию активации для процесса. Соединение Fe2O3, известное как трехокись железа или оксид железа(III), обладает достаточно высокой энергией связей между атомами железа и атомами кислорода.
Для того чтобы произошла реакция между Fe2O3 и водой, необходимо преодолеть энергетический барьер, то есть энергию активации. В данном случае энергия активации для разрыва связей воды и образования новых связей между Fe2O3 и водой намного больше, чем энергия образования связей воды с водой.
Таким образом, из-за высокой энергии связей в Fe2O3 и отсутствия возможности преодолеть энергетический барьер, реакция между Fe2O3 и водой не происходит. Данное наблюдение объясняет, почему Fe2O3 не реагирует с водой.
Окислительные свойства
Окисленное железо, образованное в результате реакции Fe2O3 с другими веществами, обычно имеет красно-коричневый цвет. Это обычно происходит при взаимодействии с веществами, способными обеспечить электроны для окисления железа.
Трехокись железа может служить окислителем в различных процессах, таких как производство стали и других металлических сплавов. Она также может использоваться в качестве катализатора в химических реакциях.
Взаимодействие с другими веществами
Оксиды железа(III) являются весьма инертными веществами и не образуют гидроксиды при взаимодействии с водой. Это связано с тем, что оксиды железа(III) уже содержат в себе замещенное кислородом, поэтому они не нуждаются в воде для образования стабильной структуры.
Однако, в особых условиях, например, при нагревании Fe2O3 с концентрированной соляной кислотой (HCl), реакция может произойти, и в результате образуется хлорид железа(III) и газообразный органический продукт. Также, Fe2O3 может реагировать с аммиаком (NH3) при нагревании, образуя ферросоединения или нитраты железа(III).
Следует отметить, что реактивность Fe2O3 может варьироваться в зависимости от условий, в которых происходит взаимодействие с другими веществами. Поэтому, возможны и другие реакции с другими реагентами, однако они не так часто встречаются.
В целом, химические свойства Fe2O3 определяются его составом и структурой, что делает его малореактивным в отношении обычных веществ, таких как вода.
Низкая растворимость
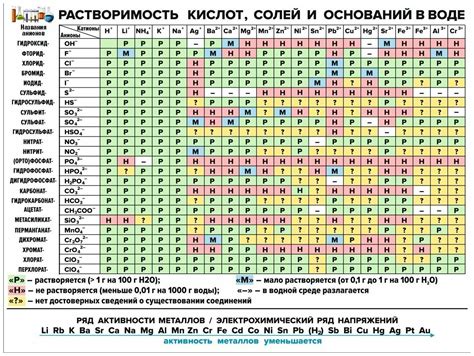
Fe2O3, или оксид железа(III), обладает низкой растворимостью в воде. Это означает, что он не диссоциирует или не реагирует с водой в заметной степени. Данный оксид имеет структуру кристаллической решетки, в которой атомы железа и кислорода тесно связаны между собой через ионные связи.
Ионные связи являются очень крепкими и, следовательно, требуют большого количества энергии для разрушения. Вода не обладает достаточной силой, чтобы разорвать ионные связи в структуре Fe2O3 и привести к его растворению.
Однако, хотя Fe2O3 не растворяется в воде, он может реагировать с некоторыми кислотами или щелочами. Например, Fe2O3 может раствориться в серной кислоте, образуя сульфат железа(III).