Соляная кислота является одним из наиболее широко используемых химических соединений в различных отраслях промышленности и лабораторий. Однако, для успешного выполнения химических реакций и добивания желаемых результатов необходимо знать и точно определить концентрацию соляной кислоты. В данной статье мы рассмотрим основные методы и советы по определению концентрации соляной кислоты.
Первым методом определения концентрации соляной кислоты является использование индикатора кислотно-основного перехода. Для этого необходимо добавить небольшое количество индикатора (например, фенолфталеина) к раствору соляной кислоты. Затем, добавляя щелочь по каплям, происходит изменение окраски раствора. Когда цвет переходит от красного к безцветному, это означает, что достигнут нужный уровень нейтрализации кислоты. Зная объём и концентрацию добавленной щелочи, можно рассчитать концентрацию соляной кислоты.
Второй метод определения концентрации соляной кислоты - использование аналитических весов. Для этого необходимо взвесить определенный объем раствора соляной кислоты, а затем измерить массу полученного раствора. Затем провести ряд глубоких аналитических взвешиваний сольфатированных препаратов в аккредитованной лаборатории для установления точной концентрации раствора. Этот метод требует использования специализированного оборудования.
Независимо от выбранного метода, важно помнить о безопасности при работе с соляной кислотой. Рекомендуется использовать защитные средства, такие как резиновые перчатки и защитные очки, а также выполнять все работы в хорошо проветриваемом помещении или под вытяжкой.
Как измерить концентрацию соляной кислоты

| Метод | Описание |
|---|---|
| Титрование | Один из наиболее распространенных методов определения концентрации соляной кислоты. Он заключается в добавлении известного объема раствора соляной кислоты к раствору с известной концентрацией щелочи, до достижения точки эквивалентности. По полученным данным можно вычислить концентрацию кислоты. |
| Использование индикаторов | При титровании соляной кислоты можно использовать различные индикаторы, которые меняют цвет в зависимости от pH раствора. Это помогает определить момент достижения эквивалентности и точно измерить концентрацию кислоты. |
| Использование pH-метра | С помощью pH-метра можно непосредственно измерить pH раствора соляной кислоты. Исходя из этого значения и использовании известных данных о pH соляной кислоты в зависимости от ее концентрации, можно определить концентрацию вещества. |
| Индуктивно связанная плазма (ИСП) | ИСП - это метод, который основан на использовании высоких температур для разложения образца и атомизации анализируемого вещества. С помощью ИСП можно определить концентрацию соляной кислоты. |
При выборе метода измерения концентрации соляной кислоты необходимо учитывать его надежность, точность и доступность. Важно также следовать инструкциям и правилам безопасности для каждого метода.
Физические свойства соляной кислоты

1. Состояние: Соляная кислота в коммерческой форме представляет собой бесцветную жидкость, которая может быть чистой или иметь слегка желтоватый оттенок. Она легко испаряется и имеет острый характерный запах.
2. Плотность: Плотность соляной кислоты зависит от ее концентрации. Чем выше концентрация кислоты, тем выше ее плотность. Например, для 37% соляной кислоты плотность составляет около 1,19 г/мл.
3. Температура кипения: У чистой соляной кислоты температура кипения составляет около 110 градусов Цельсия. Однако, при наличии примесей, точка кипения может изменяться.
4. Реакция с водой: Соляная кислота является сильным минеральным кислотным соединением. При взаимодействии с водой она образует ион водорода (H+) и ион хлорида (Cl-). Реакция соляной кислоты с водой сопровождается выделением большого количества тепла.
5. Коррозионные свойства: Соляная кислота обладает сильным коррозионным действием на металлы, особенно на железо и его сплавы. При контакте с металлами она образует хлориды и выделяет водород.
6. Степень диссоциации: Соляная кислота хорошо диссоциирует в водных растворах, что означает, что большая часть ее молекул распадается на ионы H+ и Cl-. Это свойство обусловливает кислотность раствора.
Знание физических свойств соляной кислоты помогает понять ее поведение и использовать различные методы для определения ее концентрации.
Химические свойства соляной кислоты

Во-первых, соляная кислота является сильным кислотным веществом. Она образует водородные ионы (H+) в водном растворе, что позволяет ей проявлять кислотные свойства. Это делает ее эффективным реагентом в химических реакциях, где требуется кислотная среда.
Кроме того, соляная кислота обладает высокой растворимостью в воде. Это позволяет ей легко диссоциировать в водный раствор и образовывать ионы водорода и хлорида. Растворы соляной кислоты могут быть очень концентрированными и иметь высокую степень диссоциации, что обеспечивает их эффективность в различных химических реакциях.
Также стоит отметить, что соляная кислота является оксидирующим веществом. Она способна окислять различные вещества, включая металлы, сероводород и соединения азота. Это свойство делает ее полезным химическим реагентом в различных промышленных процессах и лабораторных исследованиях.
В итоге, химические свойства соляной кислоты, такие как ее кислотность, высокая растворимость и окислительная активность, делают ее важной химической соединением в различных областях науки и промышленности.
Определение концентрации через плотность
Для начала необходимо измерить плотность исследуемого раствора, используя специальное приборное оборудование, такое как пикнометр или денсиметр. Затем плотность раствора сравнивается с таблицей, в которой указаны значения плотности для различных концентраций соляной кислоты. В результате сравнения определяется концентрация раствора.
Необходимо отметить, что точность определения концентрации через плотность зависит от качества используемого оборудования и от тщательности выполнения измерений. Также важно учитывать, что этот метод позволяет определить концентрацию соляной кислоты только в определенном диапазоне значений.
Если вам необходимо определить концентрацию соляной кислоты точнее, рекомендуется использовать другие методы анализа, такие как титрование. В каждом случае выбор метода определения концентрации зависит от доступности и точности используемого оборудования, а также от требований вашего исследования.
Определение концентрации с помощью pH-метра
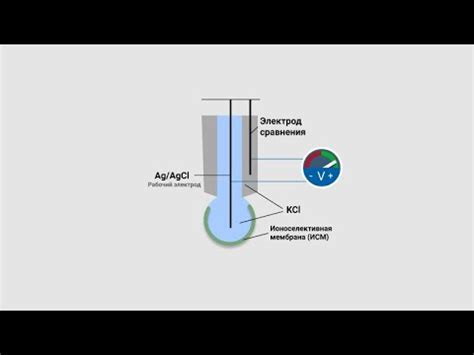
Для определения концентрации с помощью pH-метра необходимо провести следующие шаги:
1. Подготовить образец соляной кислоты, который будет использоваться для измерений. Образец должен быть достаточно разбавленным, чтобы pH-метр мог точно измерить его значение.
2. Калибровка pH-метра. Для этого необходимо использовать стандартные буферные растворы с известным pH-значением. Калибровка поможет гарантировать точность измерений.
3. Погрузите электрод pH-метра в образец соляной кислоты и дождитесь стабилизации показаний на дисплее. Запишите значение pH.
4. Сравните измеренное значение pH с таблицей, которая показывает соответствующую концентрацию соляной кислоты. Таблицы могут быть доступны в учебниках или онлайн ресурсах.
5. Учитывая, что pH является логарифмической шкалой, результаты следует интерпретировать соответствующим образом. Чем меньше pH, тем более кислотный раствор, и, следовательно, более высокая концентрация соляной кислоты.
Определение концентрации с помощью pH-метра является простым и удобным методом, который позволяет быстро и точно определить концентрацию соляной кислоты в растворе. Однако, для достижения точных результатов, необходимо правильно подготовить образец и калибровать pH-метр перед измерением.
Влияние температуры на концентрацию
Температура играет важную роль в определении концентрации соляной кислоты. При повышении температуры частички соляной кислоты обладают большей энергией, что приводит к более интенсивному движению молекул и увеличению их столкновений с растворителем.
Увеличиваясь, частота столкновений между молекулами соляной кислоты и водой сильно возрастает, что повышает вероятность образования ионов водорода и хлорида. В результате, концентрация соляной кислоты в растворе становится выше.
Следует отметить, что растворяемость соляной кислоты в воде также увеличивается при повышении температуры. Это связано с увеличением энергии движения молекул, что препятствует образованию агрегатов соляной кислоты и способствует полному распаду молекул на ионы.
Однако следует быть осторожными при работе с высокими температурами, так как соляная кислота является коррозийним веществом и может вызывать ожоги. Рекомендуется использовать специализированное оборудование и соблюдать предосторожность при проведении экспериментов.
Измерение концентрации с помощью титрования

Процесс титрования состоит из нескольких этапов:
1. Подготовка раствора известной концентрации, который будет использован для титрования. В случае с измерением концентрации соляной кислоты, раствором щелочи обычно является раствор натрия гидроксида (NaOH).
2. Подготовка пробы соляной кислоты, которая будет анализироваться. Обычно для этого используется точное количество соляной кислоты, измеренное с помощью пипетки.
3. Добавление раствора щелочи к пробе соляной кислоты с помощью бюретки, пока не будет достигнут конец титрования. Конец титрования происходит, когда эквивалентное количество исследуемой кислоты и щелочи полностью реагируют и образуется нейтральное или солевое соединение.
4. Измерение объема раствора щелочи, который был использован для достижения конца титрования. Зная начальный объем раствора щелочи и объем используемой щелочи, можно рассчитать концентрацию соляной кислоты, используя уравнение реакции.
Титрование является точным и надежным методом для определения концентрации соляной кислоты. Однако необходимо тщательно выполнить все этапы и избегать потери растворов и примесей. Результаты титрования должны быть повторены несколько раз для увеличения точности и надежности полученных данных.
Использование индикаторов в определении концентрации

Один из наиболее распространенных индикаторов, используемых для определения концентрации соляной кислоты, - это фенолфталеин. Фенолфталеин меняет свой цвет в диапазоне pH от 8,2 до 10,0, именно в этом диапазоне он становится розовым. Если раствор соляной кислоты имеет низкую концентрацию, то pH будет высоким, и при добавлении фенолфталеина раствор останется без изменений. Однако, если концентрация соляной кислоты высокая, то pH будет низким, и при добавлении фенолфталеина раствор станет розовым.
Еще один популярный индикатор, который можно использовать для определения концентрации соляной кислоты, - это лакмус. Лакмус - это природный индикатор, который изменяет свой цвет в зависимости от pH раствора. Он становится красным в кислых растворах и синим в щелочных растворах. Для определения концентрации соляной кислоты можно использовать бумажные полоски с лакмусом. Полоски помещают в раствор соляной кислоты и наблюдают за изменением цвета.
Также существуют другие индикаторы, такие как бромфенол синий и фенолрейсин. Они имеют свои особенности и используются в зависимости от целей и условий проведения определения концентрации соляной кислоты.
| Индикатор | Цвет в кислых растворах | Цвет в щелочных растворах |
|---|---|---|
| Фенолфталеин | Бесцветный | Розовый |
| Лакмус | Красный | Синий |
| Бромфенол синий | Желтый | Синий |
| Фенолрейсин | Красный | Желтый |
Использование индикаторов позволяет быстро и удобно определить концентрацию соляной кислоты без необходимости проведения сложного анализа.
Техники безопасной работы с соляной кислотой
Работа с соляной кислотой требует особой осторожности и соблюдения мер безопасности, чтобы предотвратить возможные травмы или вредные последствия для здоровья. Ниже представлены некоторые важные техники безопасной работы с соляной кислотой:
- Для начала, всегда надевайте защитный халат, респиратор, защитные очки и резиновые перчатки до начала работы с соляной кислотой.
- Размещайте соляную кислоту и все соответствующие реагенты и оборудование на кислотоустойчивой поверхности, чтобы предотвратить контакт с другими материалами.
- Используйте хорошо проветриваемое помещение или рабочую станцию под вытяжкой, чтобы предотвратить попадание паров соляной кислоты в легкие.
- Будьте осторожны при разбавлении соляной кислоты в воде - всегда добавляйте кислоту к воде, а не наоборот, чтобы избежать выплеска и брызг.
- Никогда не наклоняйтесь над емкостью с соляной кислотой и не дышите ее пары непосредственно - это может вызвать серьезные ожоги и травмы.
- После окончания работы с соляной кислотой, тщательно промойте все использованные инструменты и оборудование с водой, чтобы смыть остатки кислоты.
- Храните соляную кислоту в кислотоустойчивых емкостях, вдали от источников тепла и огня, и в помещении, недоступном для детей или посторонних лиц.
Следуя этим рекомендациям, можно существенно снизить риск возникновения несчастных случаев при работе с соляной кислотой и обеспечить безопасность на рабочем месте.
Расчеты и формулы при определении концентрации

C1V1 = C2V2
где:
C1 - начальная концентрация раствора,
V1 - объем начального раствора,
C2 - конечная концентрация раствора,
V2 - объем конечного раствора.
Также существует формула для расчета концентрации раствора с помощью плотности:
C = d * M * V
где:
C - концентрация раствора,
d - плотность раствора,
M - молярная масса растворенного вещества,
V - объем раствора.
Расчеты и формулы являются важной частью процесса определения концентрации соляной кислоты и позволяют получить точные и достоверные результаты. При выполнении расчетов необходимо быть внимательным и аккуратным, чтобы избежать ошибок и получить достоверные данные.
Советы и рекомендации при определении концентрации соляной кислоты

| 1. | Внимательно ознакомьтесь с инструкцией по работе с реактивами и оборудованием перед началом эксперимента. Используйте лабораторные очки и перчатки для безопасности. |
| 2. | Используйте качественные реагенты и оборудование, чтобы получить достоверные результаты. Проверьте срок годности реагентов. |
| 3. | Тщательно измерьте заданное количество соляной кислоты. Используйте градуированную пробирку или сосуд для точной дозировки. |
| 4. | Используйте pH-метр или лакмусовую бумажку для определения кислотности полученного раствора. Таким образом, вы сможете оценить концентрацию соляной кислоты. |
| 5. | Повторите эксперимент несколько раз, чтобы получить более точные и надежные результаты. Усредните полученные значения. |
| 6. | Избегайте контакта с кожей и слизистыми оболочками при работе с соляной кислотой. При случайном попадании раствора на кожу, немедленно промойте его большим количеством воды. |
| 7. | После окончания работы правильно утилизируйте остатки реагентов и порченые растворы в соответствии с местными правилами и нормами. |
Следуя этим советам, вы получите достоверные результаты и сможете определить концентрацию соляной кислоты с высокой точностью.