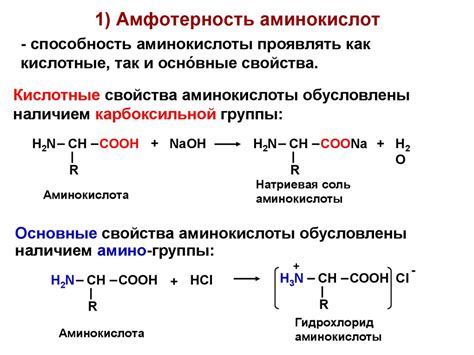
Аминокислоты являются основными строительными блоками белков - важнейших структурных и функциональных компонентов организма. Они играют особую роль в различных процессах, и их свойства обуславливаются химической структурой. Удивительно то, что большинство аминокислот обладают нейтральной реакцией среды, хотя в их структуре присутствуют функциональные группы, способные взаимодействовать с водородными и гидроксильными ионами.
Одна из научных теорий, объясняющих эту нейтральную реакцию аминокислот, основывается на концепции амфотерности. Согласно этой концепции, аминокислоты имеют способность проявлять свои амфотерные свойства в зависимости от окружающей среды. Они могут проявлять себя как кислота, образуя положительно заряженные ионы аммония, когда окружение более щелочное, и как основание, образуя отрицательно заряженные ионы карбоксилата, когда окружение более кислое.
Примеры аминокислот с нейтральной реакцией включают глицин и аланин. Глицин является самой простой аминокислотой, состоящей из всего одного атома водорода в своей боковой цепи. Поэтому глицин не имеет дополнительных функциональных групп, способных взаимодействовать с ионами. Аланин, в свою очередь, имеет боковую цепь, состоящую только из углерода и трех атомов водорода, не обладающих кислотообразующими или щелочеобразующими свойствами.
Аминокислоты и их нейтральная реакция среды: научное объяснение и примеры
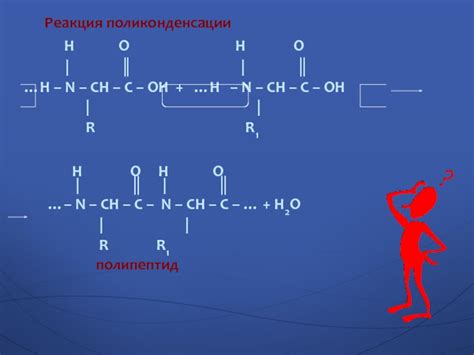
Нейтральная реакция среды означает, что аминокислота имеет равное количество положительных и отрицательных зарядов. Это происходит благодаря наличию функциональных групп, которые способны как принимать, так и отдавать протоны (H+ и OH-). Такие функциональные группы называются амфотерными, то есть они могут проявлять и кислотные, и щелочные свойства.
Примерами аминокислот с нейтральной реакцией среды являются глицин (Gly) и аланин (Ala). Оба они соответствуют нейтральному pH водных растворов и могут быть использованы в различных биологических процессах. Нейтральная реакция среды позволяет аминокислотам взаимодействовать с другими молекулами и участвовать в различных биохимических процессах в организме.
Использование аминокислот с нейтральной реакцией среды является важным аспектом в молекулярной биологии и биохимии, поскольку их свойства позволяют им выполнять различные функции в клетке и оказывать влияние на метаболические процессы.
Что такое аминокислоты
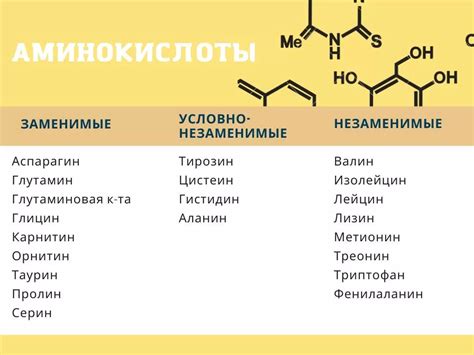
Аминокислоты состоят из аминогруппы (-NH2) и карбоксильной группы (-COOH), связанных с одной общей углеродной атомной цепью. Каждая аминокислота имеет свой собственный боковой радикал, который определяет ее свойства и функции.
В природе существует около 500 различных аминокислот, но только 20 из них встречаются в белках и играют важную роль в функционировании организма.
Аминокислоты могут быть классифицированы как незаменимые, полузаменимые и заменимые. Незаменимые аминокислоты не синтезируются организмом и должны быть поступать с пищей. Полузаменимые аминокислоты могут быть синтезированы в организме из заменимых, но их поступление с пищей также важно. Заменимые аминокислоты могут быть полностью синтезированы организмом и не требуют дополнительного поступления с пищей.
Аминокислоты играют важную роль в поддержании здоровья организма. Они участвуют в таких процессах, как образование и укрепление мышц, регуляция ферментативной активности, транспортировка и хранение питательных веществ, поддержание иммунной системы и обеспечение энергии.
Реакция аминокислот среды
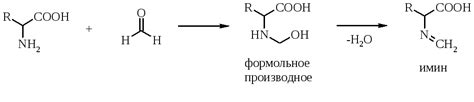
Нейтральная реакция аминокислот обусловлена их амфотерностью, то есть способностью взаимодействовать как с кислотами, так и с основаниями. Аминогруппа (-NH2) в аминокислоте может принимать протон от воды, образуя положительный ион, или отдавать протон воде, образуя отрицательный ион.
Например, рассмотрим аминокислоту глицин (C2H5NO2). Глицин имеет одну аминогруппу и одну карбоксильную группу (-COOH). При растворении в воде аминогруппа может принять протон от воды, образуя положительный ион NH3+. В то же время, карбоксильная группа может отдать протон воде, образуя отрицательный ион COO-. Эти реакции компенсируют друг друга, и в результате раствор глицина остается нейтральным.
Другой пример - аминокислота лизин (C6H14N2O2). Лизин имеет две аминогруппы и одну карбоксильную группу. При растворении в воде каждая аминогруппа может принять протон, образуя положительный ион NH3+. В то же время, карбоксильная группа может отдать протон, образуя отрицательный ион COO-. Снова, эти реакции компенсируют друг друга, и раствор лизина остается нейтральным.
Таким образом, из-за амфотерных свойств аминокислот, они имеют нейтральную реакцию среды, что делает их важными компонентами в биологических процессах и человеческом организме.
Научное объяснение

Реакция аминокислот среды зависит от ионизирующих групп, которые присутствуют в их структуре. Аминогруппа и карбоксильная группа могут выступать как кислотные и основные среды, что определяет их реакцию с окружающей средой.
При нейтральной реакции аминокислоты присутствуют в виде звеньев, при которых аминогруппа и карбоксильная группа не ионизированы. Они не образуют свободных ионов и не обладают электрическим зарядом. В таком состоянии они нейтральны по отношению к окружающей среде.
Однако, в зависимости от pH окружающей среды, аминокислоты могут проявлять свой амфотерный характер. Если окружающая среда имеет низкую кислотность, то аминогруппа аминокислот ионизируется, становясь положительно заряженной. Если среда имеет высокую кислотность, то карбоксильная группа аминокислот ионизируется, становясь отрицательно заряженной.
Примером аминокислоты с нейтральной реакцией может служить глицин, который не имеет боковой цепи и состоит только из аминогруппы и карбоксильной группы. Он является одной из самых простых аминокислот и обладает нейтральной реакцией независимо от pH окружающей среды.
Таким образом, нейтральная реакция аминокислот обусловлена ионизацией их функциональных групп в зависимости от pH окружающей среды.
Примеры нейтральной реакции аминокислот
Например, глицин имеет формулу NH2CH2COOH. В этой аминокислоте аминогруппа и карбоксильная группа находятся на разных концах молекулы. Поэтому глицин обладает нейтральной реакцией и может быть использован в телах животных и растений в процессе синтеза белка.
Аланин, с формулой NH2CH(C2H5)COOH, также входит в число аминокислот с нейтральной реакцией. Эта аминокислота, подобно глицину, играет важную роль в биохимических процессах организмов.
Помимо глицина и аланина, существует множество других аминокислот, которые также обладают нейтральной реакцией среды. Они выполняют различные функции в организме, например, участвуют в синтезе белка, играют роль в обмене веществ и обеспечивают нейтральный pH внутренней среды клетки.