Аминокислоты – это органические соединения, являющиеся основными компонентами белков. В их структуре имеются как остатки карбоксильной, так и аминогруппы. Благодаря такому строению аминокислоты обладают способностью проявлять как кислотные, так и щелочные свойства. Именно поэтому их называют амфотерными соединениями.
Остаток карбоксильной группы (-COOH) при проявлении своих кислотных свойств может отдавать протон, образуя ион карбоксилата. Ион карбоксилата имеет отрицательный заряд, поэтому он и остаток карбоксильной группы являются кислотными компонентами аминокислоты. Они обладают достаточной кислотностью для проявления реакций с щелочными соединениями.
С другой стороны, аминогруппа (-NH2) в остатке аминокислоты проявляет щелочные свойства. Она обладает базностью и способна принимать протон, образуя ион аммония (+NH3). Ион аммония имеет положительный заряд, поэтому аминогруппа и ион аммония являются основными компонентами аминокислоты. Они обладают достаточной щелочностью для проведения реакций с кислыми соединениями.
Таким образом, благодаря наличию как кислотных, так и щелочных групп в своей структуре, аминокислоты могут действовать как в качестве кислот, так и в качестве оснований. Это делает их амфотерными соединениями и позволяет им участвовать в множестве биохимических реакций, что существенно для их роли в организме живых организмов.
Химические соединения аминокислоты: амфотерные характер

Карбоксильная группа в молекуле аминокислоты обладает кислотными свойствами, так как способна отдавать протон (H+) и образовывать ион карбоксилата. В то же время, амино группа обладает щелочными свойствами и способна принимать протон и образовывать ион амидиума. Таким образом, в зависимости от условий окружающей среды, аминокислоты могут проявлять свойства как кислот, так и щелочей.
Амфотерный характер аминокислот особенно проявляется в водном растворе, где карбоксильная группа диссоциирует, образуя ион карбоксилата (-COO-) и протон (H+), тогда как амино группа принимает протон и образует ион амидиума (+NH3). В результате этой диссоциации аминокислоты приобретают положительный или отрицательный заряд, в зависимости от значения pH раствора.
Амфотерный характер аминокислот является ключевым свойством для их участия в биологических процессах организма. Благодаря этому свойству, аминокислоты могут участвовать в различных химических реакциях в биологических системах, образуя полипептидные цепочки и белки, а также выполнять функции буфера, участвуя в регуляции pH в тканях и клетках.
Особенности аминокислоты
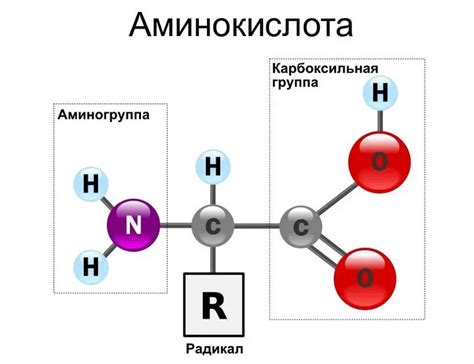
Аминокислоты классифицируются как амфотерные соединения, поскольку они могут проявлять свойства как кислоты, так и основания. Аминогруппа аминокислоты может получить протон, проявляя свойства основания. Карбоксильная группа, напротив, может отдать протон, проявляя свойства кислоты.
Особенность аминокислот состоит в том, что они имеют амфотерные свойства не только в растворе, но и в твердом состоянии. Это связано с тем, что аминогруппа и карбоксильная группа могут реагировать между собой, образуя воду и амфотерные соли. Такие реакции называются внутренней амфотерностью аминокислоты.
Благодаря своим амфотерным свойствам, аминокислоты могут взаимодействовать с другими веществами в организме, образуя различные реакции и связи. Это позволяет им выполнять важные функции, такие как участие в синтезе белков, регуляция рН организма и активация ферментов. Все это делает аминокислоты неотъемлемой частью биохимических процессов в организме человека и других живых организмов.
Кислотно-основное свойство

При повышении pH окружающей среды, аминокислота действует как слабая кислота. В этом случае карбоксильная группа (COOH) отдаёт протон, образуя карбоксилатный ион (COO-), который обладает кислотными свойствами. Таким образом, аминокислоты могут образовывать золь или соль с двумя ионными группами: кислотной и основной.
Такое кислотно-основное свойство аминокислот позволяет им участвовать в различных биохимических процессах в организме. Оно также определяет способность аминокислот взаимодействовать внутри белковой структуры, образуя водородные связи и ионные взаимодействия, что важно для их функционирования и свойств.
| Нейтральная форма | Кислая форма | Базовая форма |
|---|---|---|
| R-CH(NH2)COOH | R-CH(NH3+)COOH | R-CH(NH2)COO- |
Реакция аминокислоты с щелочью

При реакции с щелочью, аминокислоты образуют соли и вода. Гидроксид щелочи провоцирует протекание реакции, вытесняя кислотный компонент аминокислоты и образуя соль.
Например, когда аминокислота глицин, содержащая аминогруппу и карбоксильную группу, реагирует с гидроксидом натрия (NaOH), образуется натриевый глицинат, или просто глицинат NaC2H4O2:
Аминокислота глицин + гидроксид натрия → натриевый глицинат + вода
Таким образом, реакция аминокислоты с щелочью приводит к образованию соли и воды, что является типичной реакцией нейтрализации.
Реакция аминокислоты с кислотой

Протолиз аминогруппы аминокислоты возникает в результате передачи протона (H+) от кислоты на аминогруппу. При этом аминогруппа превращается в ее конъюгированную кислоту, а ион водорода присоединяется к карбоксильной группе, образуя карбоксилатный ион.
Таким образом, реакция аминокислоты с кислотой приводит к образованию беззарядной амфотерной молекулы с карбоксилатной группой и околонейтральным аминийным остатком. Это обеспечивает аминокислотам способность действовать как буферные системы, поддерживая постоянство pH внутри клеток и организма в целом.
Функции аминокислоты
В первую очередь, аминокислоты являются ключевыми элементами при синтезе белков. Они соединяются в определенном порядке, образуя цепочку, которая становится белком. Белки выполняют различные функции в организме, такие как транспортировка веществ, каталитическая активность, участие в иммунной системе и многое другое.
Кроме того, аминокислоты играют роль в обмене веществ. Некоторые аминокислоты могут быть использованы организмом в качестве источника энергии. Они могут быть разрушены, что приводит к образованию энергии. Также аминокислоты могут быть использованы для синтеза других веществ, таких как гормоны, нейротрансмиттеры и антиоксиданты.
Аминокислоты также являются важными для синтеза ДНК и РНК, которые содержат генетическую информацию организма. Они участвуют в процессе передачи генетической информации, а также в процессе регуляции генной экспрессии.
Одним из важных свойств аминокислот является их способность выступать в роли амфотерных соединений. Это означает, что аминокислоты могут действовать как кислоты и основания, способные принимать или отдавать протоны. Благодаря этому свойству, аминокислоты могут участвовать в различных биохимических реакциях, таких как реакции гидролиза, окисления и восстановления, аминирования и декарбоксилирования.
Примеры аминокислот
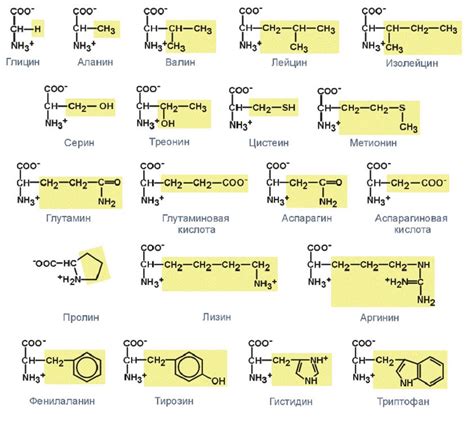
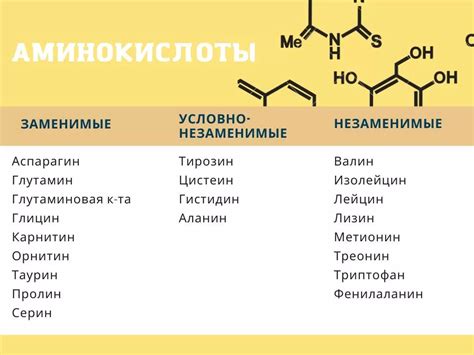
Некоторые из наиболее известных аминокислот включают:
- Глицин - самая простая аминокислота, используется во многих биологических процессах.
- Аланин - широко распространенная аминокислота, важная для обмена веществ и энергопроизводства.
- Валин - одна из ветвисто-цепных аминокислот, играет ключевую роль в синтезе белков.
- Лейцин - вторая ветвисто-цепная аминокислота, участвует в регуляции обмена веществ и синтезе белка.
- Изолейцин - еще одна ветвисто-цепная аминокислота, важная для энергопроизводства и регуляции глюкозы.
- Серин - участвует в образовании фосфолипидов и нуклеотидов, играет роль в сигнальных путях.
- Триптофан - используется для синтеза серотонина и ниацина, важных для настроения и пищеварения.
- Цистеин - участвует в образовании дисульфидных связей и антиоксидантной защите.
Это лишь некоторые примеры аминокислот, которые играют важную роль в организмах живых существ. Каждая аминокислота имеет свои уникальные свойства и функции, которые позволяют им выполнять различные задачи в биологических процессах.
Дополнительная информация

Кислотные свойства аминокислот обусловлены наличием в их структуре карбоксильной группы (-COOH), которая может отдавать протон, образуя отрицательно заряженный ион кислоты. Таким образом, аминокислоты могут проявлять кислотные свойства в реакциях с основаниями.
Основные свойства аминокислот связаны с аминогруппой (-NH2), которая способна принимать протон и образовывать положительно заряженные ионы оснований. Эти группы могут проявлять свою основность в реакциях с кислотами.
Таким образом, аминокислоты могут взаимодействовать как с кислотами, так и с основаниями, образуя соответствующие соли. Благодаря этой способности аминокислоты играют важную роль в многих биологических процессах и являются основными строительными блоками белков.