Фенолят натрия – это соль натрия и фенола, кислотная формула которой C6H5ONa. Данное соединение широко используется в промышленности, а также в лабораторных условиях. Оно обладает рядом свойств, среди которых высокая устойчивость к воде.
При контакте фенолят натрия с водой не происходит его разложение на компоненты – натрий и фенол. Это обусловлено особенностями строения и химического свойства данного вещества. Фенолят натрия образует ионный кристаллический решетчатый комплекс, в котором катионы натрия образуют каркас, а анионы фенолата занимают ячейки. Такая структура обеспечивает стабильность соединения и препятствует его растворению в воде.
Одним из аргументов в пользу того, что фенолят натрия не разлагается водой, является его растворимость в этом растворителе. Вода, будучи полярным веществом, хорошо растворяет другие полярные соединения. Но фенолят натрия – это исключение. Кристаллические соли обычно растворяются в воде путем разрушения и перераспределения ионов. Однако фенолят натрия сохраняет свою структуру и может быть растворен в других растворителях, таких как спирт или бензол.
Проблема с разложением фенолата натрия в воде

Однако, несмотря на свою высокую растворимость, фенолат натрия не разлагается в воде при обычных условиях. Это может быть проблемой при его использовании, особенно если требуется удаление или обработка отходов, содержащих этот материал.
Причина такого поведения фенолата натрия заключается в его структуре. Это соединение образует мощные и стабильные ионные связи с натрием, которые обеспечивают его кристаллическую структуру и растворимость в воде. Эти связи очень сильные и требуют большого количества энергии для разрыва.
Кроме того, фенолат натрия обладает невысокой кислотностью. Это означает, что его pH недостаточно низкий для активного реагирования с водой и разложения. Вода не обладает достаточной силой или реактивностью для нарушения связей между фенолатом натрия и натрием.
В связи с этим, если требуется разложить фенолат натрия в воде, необходимо применять другие методы, такие как использование сильных кислот или щелочей, повышенных температур или применение более активных реагентов. Это может быть сложно и дорогостояще, поэтому важно тщательно планировать и контролировать использование фенолата натрия для минимизации его потенциального воздействия на окружающую среду.
Молекулярная структура фенолата натрия
Фенолат (C6H5O-) обладает ароматическими свойствами и представляет собой отрицательно заряженный ион. Этот ион образуется путем замены одного атома водорода в молекуле фенола (C6H6O) на ион натрия (Na+). Таким образом, молекула фенолата натрия содержит шестичленное ароматическое кольцо из атомов углерода и атома кислорода, а также ион натрия, который находится около кольца.
Ионы натрия (Na+) в фенолате натрия играют роль положительно заряженных катионов, которые обеспечивают электрическую нейтральность соединения в целом. Ионы натрия окружены отрицательно заряженными ионами фенолата и взаимодействуют с ними через электростатические силы притяжения.
Молекулярная структура фенолата натрия обуславливает его свойства и поведение в растворах. Вода не способна разлагать фенолат натрия, так как молекулы воды не могут разорвать электростатические связи между ионами натрия и фенолата. Это объясняет стабильность фенолата натрия в водных растворах и его способность сохранять свою молекулярную структуру.
Водородные связи и их влияние на разложение фенолата натрия
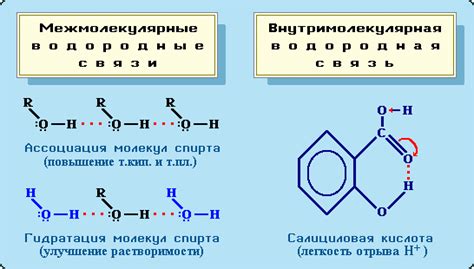
Однако, в отличие от других фенолатов, фенолат натрия не разлагается водой. Это связано с особенностями структуры и связей в молекуле фенолата. Фенолат и вода могут образовывать водородные связи - слабые, но важные силы притяжения между молекулами.
Водородные связи возникают между атомами кислорода воды (H2O) и атомами водорода в фенолате натрия (NaOC6H5). Эти связи обеспечивают стабильность и прочность структуры фенолата, что препятствует его разложению под влиянием воды.
Сила водородной связи зависит от ряда факторов, включая электроотрицательность атомов и количество связанных водородных атомов. В случае с фенолатом натрия, существенную роль играет ионный характер связи между натрием и фенолатом.
Таким образом, водородные связи в структуре фенолата натрия играют важную роль в его устойчивости к разложению в воде. Это объясняет почему фенолат натрия не разлагается при взаимодействии с водой и остается стабильным в растворе.
Реакция фенолата натрия с водой и ее последствия
Фенолат натрия не разлагается вода, поскольку реакция между фенолатом натрия и водой не является спонтанной и не происходит сами по себе. Для этого требуется наличие дополнительных реагентов или изменение условий реакции.
Однако, если фенолат натрия подвергается воздействию кислоты, происходит реакция нейтрализации, в результате которой образуются фенол и натриевая соль кислоты. Реакция идет следующим образом:
C6H5ONa + HCl → C6H5OH + NaCl
Полученный фенол может проявить свои физико-химические свойства, например, обладать характерным запахом и быть растворимым в жирных растворителях. Он также может использоваться в различных производственных процессах и химических реакциях.
Поэтому, реакция фенолата натрия с водой не является существенной химической реакцией, и не оказывает значительного влияния на окружающую среду, правда, и его применение в чистом виде не находит широкого применения.
Влияние pH и температуры на разложение фенолата натрия в воде
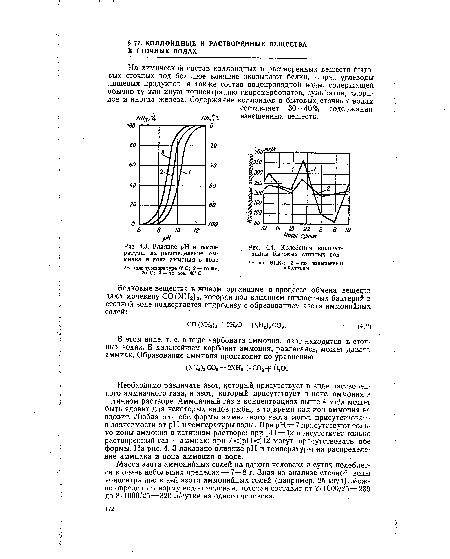
Фенолат натрия представляет собой соль фенола и натрия, которая широко используется в промышленности. Эта соль обладает несколькими уникальными свойствами, включая высокую щелочность и стабильность в водных растворах. Однако, разложение фенолата натрия может происходить при определенных условиях.
Влияние pH на процесс разложения фенолата натрия в воде является одним из ключевых факторов. Фенолат натрия обладает высокой стабильностью в щелочной среде с высоким значением pH, так как ион Н О высоко стабилен при повышенном pH. Однако, при уменьшении pH воды до кислотного значения, ионизированный фенолат натрия может протонироваться, что приводит к разложению соли. Поэтому, в условиях низкого pH, фенолят натрия может быть разрушен в водной среде.
Температура также оказывает влияние на разложение фенолата натрия. При повышении температуры воды, скорость разложения фенолата натрия возрастает. Это связано с увеличением энергии молекул, что способствует более эффективному протеканию химических реакций разложения.
Таким образом, pH и температура играют важную роль в разложении фенолата натрия в воде. Высокое pH способствует стабильности соли, тогда как низкое pH и повышенная температура способствуют ее разложению. Понимание этих факторов важно для контроля и управления разложением фенолата натрия в промышленных и экологических процессах.