Газы - это состояние вещества, которое отличается от твердого и жидкого состояний. Они не имеют формы и постоянного объема, а также обладают свойством легкости и способности распространяться в пространстве без определенного направления. Эти особенности газового состояния связаны с их молекулярной структурой и поведением молекул вещества.
В газовом состоянии молекулы вещества двигаются хаотично, сталкиваются друг с другом и с поверхностями, создавая давление на сосуды, в которых находятся. Такое движение молекул обусловлено их высокой энергией, которая позволяет им преодолевать силы притяжения друг к другу и свободно перемещаться в пространстве. Поэтому газы не имеют постоянной формы и объема.
В то же время, газы могут заполнять все имеющееся пространство, равномерно распределенные по всему объему сосуда. Их объем может изменяться в зависимости от давления и температуры. При изменении давления молекулы газа могут сжиматься или расширяться, что влияет на его объем. Также при нагревании газы расширяются, а при охлаждении - сжимаются.
Изучение свойств газов имеет важное практическое значение во многих областях науки и техники. Понимание процессов, происходящих с газами, помогает разрабатывать эффективные системы отопления, кондиционирования и хранения газов, а также предсказывать и анализировать изменения состояния вещества при различных условиях. Таким образом, изучение газового состояния вещества имеет большое значение для практического применения в различных областях науки и промышленности.
Свободное движение молекул
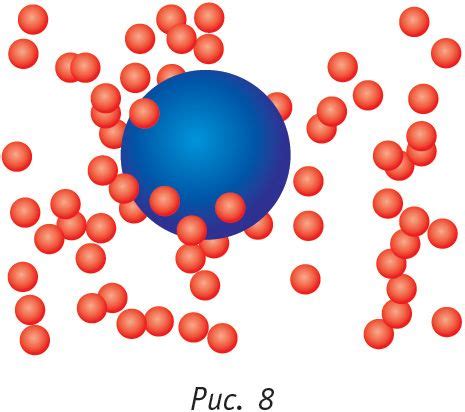
Молекулы газа находятся в непрерывном движении, изменяя свое направление и скорость с каждым столкновением с другими молекулами и стенками сосуда. Это свободное движение молекул позволяет газу занимать весь доступный объем сосуда и не иметь постоянной формы.
Молекулы газа взаимодействуют между собой с помощью слабых сил притяжения или отталкивания. При высоких температурах и низких давлениях эти силы имеют малое влияние, и молекулы с легкостью прятываются друг от друга, не образуя упорядоченных структур. Это позволяет газу не иметь постоянного объема.
Также, свободное движение молекул газа позволяет ему заполнять любую форму сосуда, в котором он находится. Если изменить форму сосуда, молекулы газа просто приспособятся к новым условиям и будут заполнять новый объем также свободно, как и прежде.
Свободное движение молекул является одной из основных особенностей газового состояния вещества и объясняет, почему газы не имеют формы и постоянного объема.
Отсутствие межмолекулярных сил притяжения

В отличие от твердого и жидкого состояний, где силы притяжения между молекулами существенно влияют на их движение и фиксируют их в определенном объеме, газы характеризуются высокой подвижностью и способностью заполнять все доступное пространство.
Интермолекулярные силы, обеспечивающие сцепление частиц в жидкостях и твердых телах, основаны на притяжении положительно и отрицательно заряженных частей молекул, а также на других типах взаимодействий, таких как силы Ван-дер-Ваальса. Однако, в газовом состоянии расстояния между молекулами настолько велики, что эти силы становятся незначительными и не оказывают существенного влияния на движение частиц.
Следствием этого является отсутствие постоянной формы и объема у газовой среды. Молекулы и атомы газа свободно перемещаются в пространстве, сталкиваясь друг с другом и со стенками сосуда, в котором находится газ. Из-за отсутствия сильной силы притяжения, они могут свободно двигаться и изменять свою скорость и направление. В результате газ занимает любую ему доступную область, не сохраняя постоянной формы и объема.
Высокая подвижность газовых частиц
Газы представляют собой агрегатное состояние вещества, в котором его частицы находятся в постоянном хаотическом движении. Их высокая подвижность объясняется низкой силой притяжения между ними.
Молекулы газов воздействуют друг на друга и окружающую среду через интермолекулярные силы. Однако эти силы для газов незначительны по сравнению со силами притяжения в твёрдых или жидких веществах.
Частицы газа обладают высокой кинетической энергией и, поэтому, движутся с большой скоростью во всех направлениях. Они свободно перемещаются в пространстве до тех пор, пока не столкнутся с другими частицами или с преградами.
Из-за этой свободы перемещ
Газы наполняют все доступное пространство
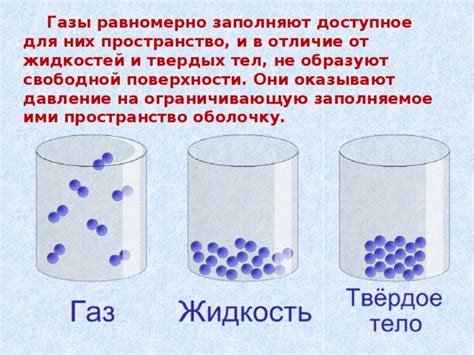
Так как молекулы газов находятся на значительном расстоянии друг от друга, они могут свободно перемещаться во всех направлениях. Благодаря этому свойству газы наполняют все доступное им пространство, полностью заполняя сосуды и контейнеры, в которые они помещены.
Из-за свободного перемещения молекул газы также обладают высокой подвижностью. Они могут равномерно распространяться и заполнять среду, в которую они попадают. Этим объясняется способность газов к диффузии – распространению вещества через среду.
Таким образом, газы не имеют формы и постоянного объема, так как их молекулы свободно перемещаются и наполняют все доступное пространство. Это обуславливает их способность равномерного распределения и диффузии.
Свойства газов при изменении температуры и давления
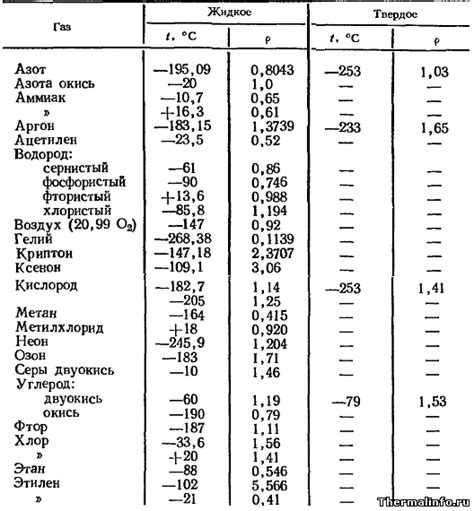
Газы обладают различными свойствами, которые изменяются в зависимости от температуры и давления, с которыми они взаимодействуют. Ниже перечислены некоторые из этих свойств:
- Объем: Газы не имеют постоянного объема и могут расширяться или сжиматься в зависимости от изменения давления. При увеличении давления газ сжимается, занимая меньший объем, а при уменьшении давления газ расширяется, занимая больший объем.
- Давление: Давление газа определяется силой, с которой газ молекулы сталкиваются с поверхностью, на которую действует газ. При увеличении температуры газовые молекулы приобретают большую скорость и сталкиваются с поверхностью с большей силой, что приводит к увеличению давления.
- Температура: Температура является мерой средней кинетической энергии газовых молекул. При повышении температуры молекулы газа двигаются быстрее, что приводит к увеличению их кинетической энергии и давления.
- Плотность: Плотность газа определяется отношением его массы к объему. При увеличении давления или уменьшении объема плотность газа увеличивается.
- Распределение скоростей: В газе существуют молекулы с различными скоростями. При повышении температуры распределение скоростей газовых молекул становится более равномерным.
Таким образом, изменение температуры и давления оказывает значительное влияние на свойства газов, включая их объем, давление, плотность и распределение скоростей. Эти свойства являются основой для понимания поведения газов и используются в различных областях науки и техники.
Влияние объема и формы твердого контейнера на газы
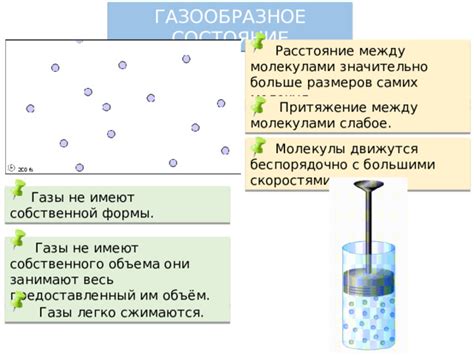
Однако, форма и объем твердого контейнера, в котором содержится газ, могут оказать влияние на свойства газа и его поведение.
Во-первых, объем твердого контейнера может оказывать влияние на давление газа. В соответствии с законами газовой динамики, давление газа прямо пропорционально объему контейнера. То есть, при увеличении объема контейнера, давление газа внутри него снижается, а при уменьшении объема - повышается.
Во-вторых, форма твердого контейнера может оказывать влияние на равномерность заполнения газом всего объема контейнера. Например, если контейнер имеет необычную форму с узкими участками или заглублениями, то газ может сближаться или скапливаться в этих областях, не полностью заполняя всю доступную ему площадь. Это может привести к нарушению равновесия внутри контейнера и неравномерности распределения давления газа.
Учитывая эти факторы, при хранении и транспортировке газов важно учитывать не только их объем, но и форму твердого контейнера. Оптимальный выбор объема и формы контейнера позволит обеспечить равномерное заполнение газом, сохранение стабильного давления и безопасность его использования.
| Фактор | Влияние |
|---|---|
| Объем контейнера | Прямо пропорциональное влияние на давление газа |
| Форма контейнера | Может повлиять на равномерность заполнения газом и распределение давления |
Особенности газовой среды для передвижения частиц
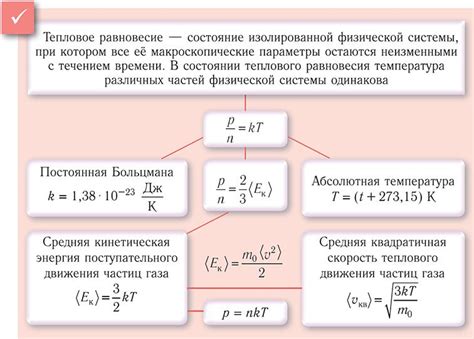
Передвижение частиц в газе происходит за счет их высокой энергии и случайных соударений с другими частицами и стенками сосуда. При этом, каждая газовая частица движется по прямолинейной траектории до тех пор, пока не столкнется с другой частицей или со стенкой сосуда.
Эта способность газа свободно перемещаться позволяет ему заполнять пространство любой формы и размера. Независимо от формы сосуда, газовые частицы заполняют его полностью и равномерно. Это объясняет почему газы не имеют формы и постоянного объема.
Еще одной особенностью газовой среды является то, что она усваивает объем своего сосуда. Это значит, что объем газа меняется в зависимости от объема сосуда, в котором он находится. Когда объем сосуда увеличивается, газ расширяется, а когда объем сосуда сужается, газ сжимается.
Таким образом, особенности газовой среды для передвижения частиц включают свободное перемещение частиц, способность газа заполнять пространство любой формы и размера, а также изменение объема газа в зависимости от объема сосуда.