Газы являются одной из основных форм вещества, которые мы встречаем в нашей повседневной жизни. Они имеют уникальные свойства, которые делают их такими переменчивыми и интересными для изучения. От легких и невесомых до тяжелых и сильно раздражающих, газы могут существовать в самых разных состояниях и проявлять разнообразные свойства.
Газы представляют собой состояние вещества, в котором его частицы свободно движутся в пространстве и не связаны между собой сильными силами притяжения. Это позволяет газам занимать любую форму и объем сосуда, в котором они находятся. Благодаря этим свойствам газы легко расширяются и сжимаются при изменении температуры и давления. Также они обладают высокой мобильностью и способностью быстро перемещаться в пространстве, что делает их трудными для контроля и управления.
Кроме того, газы обладают специфическими физическими и химическими свойствами, такими как низкая плотность, хорошая проводимость тепла и электричества, возможность растворяться в других веществах и образовывать с ними смеси. Их поведение под воздействием внешних условий и различных факторов может быть очень сложным и неоднозначным. Все это делает газы не только уникальными, но и очень переменчивыми в своих свойствах и реакциях.
Почему газы меняют свои свойства?

Одной из причин изменения свойств газов является изменение температуры. При повышении температуры молекулы газа получают больше энергии и начинают двигаться быстрее. Это приводит к увеличению давления и объема газа. Например, газ может переходить из жидкого состояния в газообразное при нагревании.
Давление также влияет на свойства газов. При увеличении давления молекулы газа начинают сталкиваться чаще, что приводит к увеличению плотности и уменьшению объема. Это может происходить, например, при сжатии газа в цилиндре.
Состав газа также влияет на его свойства. Различные газы имеют разные молекулярные составы, что приводит к различным химическим реакциям и физическим свойствам. Например, один газ может быть более легким и тяжелым, чем другой.
Взаимодействие газов с другими веществами также может изменять их свойства. Например, газы могут растворяться в жидкостях или реагировать с ними, что приводит к изменению их химических и физических свойств.
| Фактор | Влияние на свойства газа |
|---|---|
| Температура | Изменение давления и объема газа |
| Давление | Изменение плотности и объема газа |
| Состав газа | Различные химические и физические свойства |
| Взаимодействие с другими веществами | Изменение химических и физических свойств |
Все эти факторы взаимно влияют друг на друга и могут приводить к различным изменениям свойств газов. Именно благодаря этой переменчивости газы находят широкое применение в разных отраслях науки и промышленности.
Влияние температуры на состояние газов

Когда температура увеличивается, молекулы газа начинают двигаться быстрее и расширяться в объеме. Это приводит к увеличению давления газа. Если температура продолжит расти, то молекулы будут двигаться еще более активно, и газ может перейти в состояние плазмы.
С другой стороны, при снижении температуры молекулы газа начинают двигаться медленнее и сближаться друг с другом. Это приводит к сжатию газа и уменьшению его объема. Если температура продолжит падать, то газ может перейти в состояние жидкости или даже твердого тела.
Таким образом, изменение температуры может приводить к изменению состояния газов. Это является одной из причин, почему газы такие переменчивые и имеют широкий диапазон свойств.
Различные свойства газов в зависимости от давления
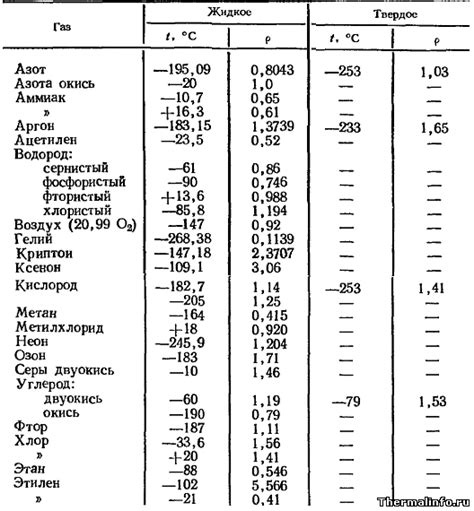
При повышении давления газы обычно сжимаются и занимают меньший объем. Это объясняется тем, что давление действует на молекулы газа, уменьшая расстояние между ними и прижимая их друг к другу. В результате увеличения давления газ становится плотнее и его молекулы движутся с более высокой скоростью.
Однако при достаточно высоком давлении газ может перейти в другое агрегатное состояние – жидкость или даже твердое вещество. Это обусловлено тем, что при сжатии газа наступает момент, когда силы взаимодействия между молекулами становятся настолько сильными, что газ перестает обладать свойствами газообразного состояния и его молекулы начинают формировать упорядоченную структуру.
Существуют также газы, которые не подчиняются обычным законам и проявляют необычные свойства, когда давление изменяется. К ним относятся, например, инертные газы, такие как гелий и неон. Их молекулы очень маленькие и слабо взаимодействуют между собой, поэтому они сохраняют свои газообразные свойства даже при очень высоких давлениях.
Таким образом, давление оказывает существенное влияние на свойства газов. В зависимости от давления газ может сжиматься, переходить в другие состояния или сохранять свои газообразные свойства. Понимание этого влияния позволяет лучше понять и описать поведение газов в различных условиях.
Газы и их взаимодействие с другими веществами
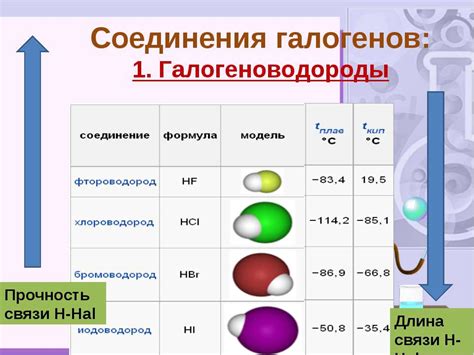
Газы могут взаимодействовать с другими веществами посредством различных процессов. Одним из таких процессов является растворение газов в жидкостях. Например, когда углекислый газ растворяется в воде, образуется газообразная смесь. Это взаимодействие используется в содовых напитках, где газировка добавляется в жидкость для создания пузырьков.
Газы также могут вступать в химические реакции с другими веществами. Например, когда кислород взаимодействует с горючим веществом, таким как бензин или уголь, происходит окисление и выделение энергии. Это основной принцип работы двигателей внутреннего сгорания и средств пожаротушения.
Газы также могут проявлять свои переменчивые свойства при сжатии и расширении. Если газ сжимается, его объем уменьшается, а давление увеличивается. Это явление можно использовать в пневматических системах для передачи силы и энергии. Например, воздушные подушки в автомобилях используют сжатый воздух для амортизации ударов.
С другой стороны, при расширении газа его объем увеличивается, а давление уменьшается. Это принцип используется во многих технологических процессах, таких как работа газовых турбин и холодильных систем.
Таким образом, переменчивость газов обусловлена их особенностями состояния, а также их взаимодействием с другими веществами. Изучение этих свойств позволяет нам понять основные процессы, происходящие в природе и применять газы в различных технологиях и промышленных процессах.
Что оказывает влияние на плотность газов?

Во-первых, температура газа оказывает существенное влияние на его плотность. При повышении температуры молекулы газа получают больше энергии, в результате чего они начинают двигаться быстрее и сталкиваться чаще. Это приводит к увеличению объема газа и, следовательно, к уменьшению его плотности. Наоборот, при понижении температуры газ становится менее движимым, его молекулы движутся медленнее и сталкиваются реже, что приводит к увеличению плотности газа.
Во-вторых, давление также влияет на плотность газа. При повышении давления газ сжимается, объем его уменьшается, а плотность увеличивается. Снижение давления, напротив, приводит к расширению газа и увеличению его объема, что приводит к уменьшению плотности.
Кроме того, состав газовой смеси может влиять на ее плотность. Различные газы имеют разные молекулярные массы, что оказывает влияние на их плотность. Газы с большей молекулярной массой, как правило, имеют большую плотность, чем газы с меньшей молекулярной массой.
Таким образом, плотность газа зависит от его температуры, давления и состава газовой смеси. Эти факторы взаимосвязаны и могут быть модифицированы для контроля плотности газа в различных условиях.
Зависимость газов от состава и структуры

Состав газа может включать различные химические элементы и соединения. Например, атмосферный воздух состоит преимущественно из азота, кислорода и небольших количеств других газов, таких как углекислый газ, аргон и водяной пар. Наличие или отсутствие определенных элементов или соединений может существенно влиять на свойства газа.
Структура газа описывает расположение и движение его молекул. Газы могут быть одноатомными, такими как аргон или неон, или состоять из молекул, состоящих из двух или более атомов, таких как водяной пар или углекислый газ. Структура газа может определять такие свойства, как плотность, теплопроводность и вязкость.
Зависимость газов от состава и структуры проявляется в различных явлениях. Например, смесь газов может проявлять неидеальное поведение, что может быть объяснено взаимодействием и взаимным влиянием молекул разных газов. Также структура газа может влиять на его способность к смешиванию с другими газами или растворению в жидкости.
| Свойство газа | Зависимость от состава и структуры |
|---|---|
| Плотность | Зависит от массы и объема газа, которые в свою очередь зависят от типа атомов или молекул, из которых состоит газ. |
| Теплопроводность | Зависит от способности молекул газа передавать тепло через соударения друг с другом. Структура газа определяет вероятность и эффективность таких соударений. |
| Вязкость | Зависит от взаимодействия молекул газа друг с другом. Структура газа может определить степень взаимодействия и, следовательно, вязкость газа. |
Понимание зависимости газов от состава и структуры является важным для практического применения газов в различных областях, таких как промышленность, медицина и наука. Изучение этих зависимостей позволяет оптимизировать процессы и создавать новые материалы и технологии на основе газов.