В мире науки и атомной физики существует удивительное явление – совпадение массы атома и массы его ядра. Несмотря на то, что эти два компонента атома имеют разные размеры и различную структуру, их массы оказываются равными. Это явление, которое сразу бросается в глаза, требует объяснения и глубокого понимания. Ведь казалось бы, каким образом можем быть согласованы и взаимозаменяемы массы этих двух элементов?
Один из ключевых ответов на этот вопрос связан с основными свойствами частиц, составляющих атом. Ядро атома содержит протоны и нейтроны, которые являются задачей. Они обладают массой и некоторым зарядом, который притягивает электроны и удерживает их вокруг ядра. Само по себе ядро основано на принципе сохранения энергии и массы.
В соответствии с принципом сохранения массы, сумма масс протонов и нейтронов в ядре часто называется массовым числом ядра. Другими словами, масса ядра возникает как результат сложения масс его составляющих частиц. И так как протоны и нейтроны являются независимыми частицами в атоме, их массы складываются и дают итоговую массу ядра, равную массе атома в целом.
Загадка массы атома

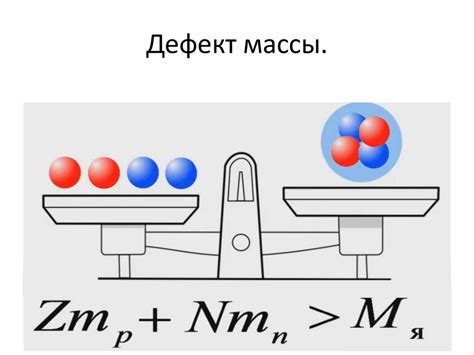
Вся масса атома, как известно, сконцентрирована в ядре. Именно в ядре атома находятся протоны и нейтроны – элементарные частицы, обладающие массой. Если сложить массы всех протонов и нейтронов в ядре, мы получим массу ядра. Однако, при измерении массы атома, получается значение, которое отличается от ожидаемого значения массы ядра.
Это можно объяснить с помощью понятия атомной массы. Атомная масса – это средняя масса атомов элемента, учитывающая их изотопический состав. Изотопы – это атомы одного и того же элемента, но с разным количеством нейтронов в ядре. Изотопы имеют разные массы, и взвешенное среднее значение массы атомов учитывает их доли в природе.
Таким образом, масса атома может отличаться от массы ядра из-за наличия разных изотопов этого элемента. Средняя масса атома учитывает все изотопы и их относительное количество в природе. Поэтому, в зависимости от изотопического состава, масса атома может быть как больше, так и меньше массы ядра.
Загадка массы атома имеет решение в атомной массе и изотопах, которые вносят свой вклад в общую массу атома и делают ее отличной от массы ядра.
Раскрытие тайны массы ядра
Масса ядра атома и его общая масса определяются с помощью сложных физических и математических формул. Один из ключевых элементов, к которым относятся протоны и нейтроны, создающие ядро атома, играет важную роль в этом процессе.
Несмотря на то, что протоны и нейтроны имеют существенно различающиеся свойства, их масса оказывается примерно одинаковой. Это факт оказывается весьма необычным для обычного человека, ведь протоны заряжены положительно, а нейтроны не имеют заряда вовсе.
Чтобы объяснить это явление, ученые прибегают к формулировкам теорий, исследующих элементарные частицы, и привлекают к этому квантовую физику. Одна из гипотез состоит в том, что существует нечто, называемое кварками, которые составляют протоны и нейтроны и придают им массу. Это предположение возникает из расчетов и экспериментов, и хотя ни один кварк пока что не был наблюден непосредственно, их существование находится на уровне предположений и допущений.
Таким образом, тайна массы ядра до сих пор является предметом исследований мировых ученых, и пока нет однозначного ответа на вопрос, почему масса ядра совпадает с массой атома. Более того, научное понимание этого явления может продолжить эволюцию с развитием науки и появлением новых экспериментальных данных.
Роль энергии связи в вопросе массы

С одной стороны, масса ядра и масса атома на самом деле не совпадают. Масса ядра всегда меньше массы атома ввиду того, что в атоме присутствуют электроны, которые также вносят свой вес в общую массу атома.
Однако, важно понимать, что вопрос здесь не в точных значениях массы, а в разнице между массой ядра и массой атома. Эта разница объясняется энергией связи, которая существует между нуклонами в ядре атома.
Энергия связи представляет собой энергию, которая необходима для разделения нуклонов друг от друга. При образовании ядра атома, протоны и нейтроны притягиваются друг к другу с помощью сильного ядерного взаимодействия, создавая энергию связи.
Это взаимодействие обеспечивает стабильность ядра и препятствует его распаду. Однако, энергия связи также вносит свой вклад в массу ядра. Согласно известной формуле Эйнштейна E=mc², энергия связи имеет влияние на массу ядра, поскольку она эквивалентна массе.
Таким образом, разница между массой ядра и массой атома связана с энергией связи, которая определяет стабильность и свойства ядра. Это явление имеет важное значение не только для физики, но и для других наук, таких как химия и астрофизика.