Смешение спирта и воды - процесс, который часто встречается в химических лабораториях и промышленности. Но почему при смешивании объем спирта и воды уменьшается? Для понимания этого явления необходимо обратиться к особенностям взаимодействия молекул спирта и воды.
Сам по себе спирт - гидрофильное вещество, т.е. он легко смешивается с водой. В то же время вода - гидрофобное вещество. Именно поэтому при смешении спирта и воды происходит изменение объема. Водные молекулы окружают молекулы спирта, формируя более плотную структуру. Это объясняет уменьшение объема при смешивании спирта и воды.
Кроме того, спирт и вода образуют азеотропную смесь при определенном соотношении компонентов. Для этилового спирта и воды это соотношение равно примерно 95,4% этилового спирта и 4,6% воды. В этой смеси спирт и вода уже не могут разделиться на составляющие компоненты без применения специальных методов.
Итак, ответ на вопрос, почему объем спирта и воды уменьшается при смешении, можно найти в гидрофильных и гидрофобных свойствах этих веществ. Образуя более плотную структуру и образуя азеотропную смесь, спирт и вода претерпевают изменение объема, что обусловливает резкое изменение их плотности.
Процесс смешения спирта и воды: почему объем уменьшается?
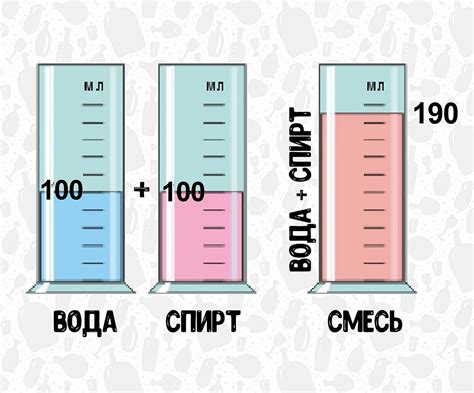
При смешивании спирта и воды происходит образование водно-спиртовой смеси, которая обладает своими физическими свойствами. Причина уменьшения объема связана с разницей в молекулярной структуре спирта и воды.
Молекулы воды образуют сеть водородных связей, что делает ее более плотной по сравнению со спиртом. Когда спирт и вода смешиваются, молекулы спирта проникают в структуру воды, нарушая сеть водородных связей. В результате происходит сжатие воды, что приводит к уменьшению объема смеси.
Кроме того, взаимодействие молекул спирта и воды приводит к образованию гидратов - структур, в которых молекула спирта окружена молекулами воды. Процесс образования гидратов также приводит к уменьшению объема смеси.
Таким образом, объем смеси спирта и воды уменьшается из-за взаимодействия молекул спирта и воды, а также образования гидратов. Это явление имеет большое значение в различных отраслях промышленности и науки, где точное смешивание жидкостей играет важную роль.
Молекулярные взаимодействия

При смешении спирта и воды происходят сложные молекулярные взаимодействия, которые определяют изменение объема смеси. Молекулы спирта и воды взаимодействуют друг с другом за счет положительных и отрицательных зарядов, образуя водородные связи.
Молекулы спирта имеют гидрофобные хвосты, которые не образуют водородные связи с молекулами воды. Это приводит к образованию кластеров спирта в смеси, где молекулы спирта так сказать "обнимаются" друг с другом. В результате этого образуется более плотная структура, которая занимает меньший объем.
Таким образом, объем смеси спирта и воды уменьшается из-за особенностей молекулярных взаимодействий. Это явление объясняет многое, например, почему ледное пиво занимает больше места, чем обычное пиво, потому что при замерзании образуются кристаллические структуры воды, которые занимают больший объем.
Химическая природа спирта и воды
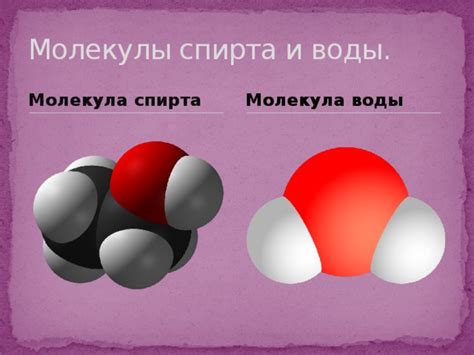
Важное отличие между спиртом и водой заключается в их полярности. Спирт является полярным соединением, потому что гидроксильная группа в его структуре создает разность зарядов. Вода также является полярным соединением из-за разности электроотрицательности атомов кислорода и водорода.
Когда спирт и вода смешиваются, происходят интермолекулярные взаимодействия между молекулами спирта и воды. Водородные связи образуются между положительно заряженными водородными атомами воды и отрицательно заряженными кислородными атомами спирта. Эти взаимодействия приводят к формированию кластеров или клубков, которые подавляют движение отдельных молекул вещества.
В результате образуются молекулярные ассоциации, которые делают смесь спирта и воды менее плотной, чем смеси двух самих веществ. Сущность этого эффекта заключается в возникновении дополнительных связей между молекулами, которые ограничивают их движение и уменьшают объем смеси.
Это уменьшение объема смеси спирта и воды также объясняется влиянием взаимодействий на межмолекулярное пространство. Кластеры молекул спирта и воды занимают больше места, чем отдельные молекулы каждого вещества, поэтому объем смеси уменьшается по сравнению с объемом отдельных компонентов.
Химическая природа спирта и воды, их полярность и взаимодействия между молекулами являются ключевыми факторами, определяющими уменьшение объема при смешении.
Образование водородных связей

В случае смешения спирта (этанола) и воды, происходит взаимодействие молекул двух веществ. Кислородный атом воды, являющийся частично отрицательно заряженным, притягивает атом водорода, который частично положительно заряжен. Таким образом, образуется водородная связь между молекулами спирта и воды.
Это взаимодействие приводит к уменьшению объема смеси, так как образование водородных связей приводит к формированию более компактной структуры. Молекулы спирта и воды становятся ближе друг к другу и занимают меньше пространства.
Именно образование водородных связей приводит к возможности смешивания веществ с разными плотностями, так как эти связи компенсируют различия в плотности молекул. Благодаря водородным связям вода и спирт образуют однородную смесь, несмотря на различия в их физических свойствах.
Изменение плотности смеси
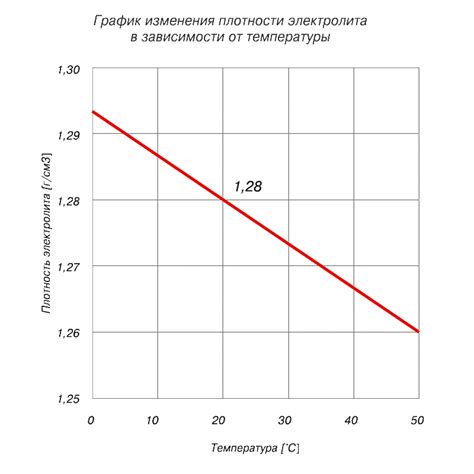
При смешении спирта и воды их объем уменьшается, что влияет на плотность получившейся смеси. Это происходит из-за наличия межмолекулярных сил притяжения между молекулами вещества.
Вода имеет более высокую плотность, чем спирт, поэтому при смешении объем спирта в смеси уменьшается, чтобы уравнять свою плотность с плотностью воды. Также влияние на объем смеси оказывает смешение молекул воды и спирта, что приводит к более плотной упаковке молекул вещества.
Изменение плотности смеси может иметь значительные физические и химические последствия. Например, плотность смеси спирта и воды может влиять на теплопроводность, растворимость веществ, а также на их физические свойства, такие как плотность пара или точка кипения.
Таким образом, при смешении спирта и воды объем обоих веществ уменьшается, а плотность смеси изменяется в зависимости от соотношения компонентов и сил притяжения между молекулами.
Термодинамические законы

В объяснении уменьшения объема спирта и воды при их смешении важную роль играют термодинамические законы.
Первый закон термодинамики, также известный как закон сохранения энергии, утверждает, что энергия не может быть создана или уничтожена, а может только переходить из одной формы в другую. При смешении спирта и воды происходит обмен энергией между молекулами веществ, что может привести к изменению их объема.
Второй закон термодинамики гласит, что энтропия замкнутой системы всегда стремится увеличиваться. Энтропия – это мера хаоса в системе. При смешении спирта и воды, молекулы образуют новое состояние, возможно, более хаотичное, чем их исходное состояние. Это влияет на межмолекулярные силы и, следовательно, на объем смеси.
Таким образом, смешение спирта и воды приводит к перераспределению энергии и межмолекулярных сил в системе, что может привести к уменьшению объема смеси. Это явление может быть объяснено и термодинамическими законами и химическими свойствами смешиваемых веществ.
Отличия в поларности молекул
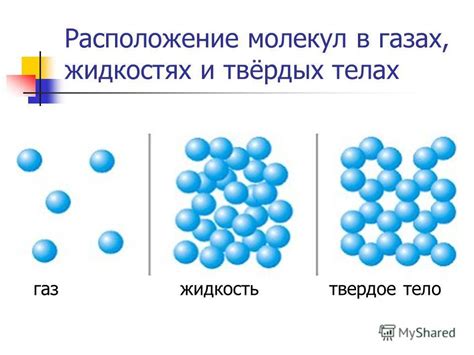
Молекулы спирта (например, этанола) обладают полярными свойствами. У них имеется электронегативный атом, такой как кислород или азот, который притягивает электроны к себе. Поэтому в молекулах спирта образуется электронная область повышенной плотности. Это делает их полюсными, или полярными, молекулами.
С другой стороны, молекулы воды также обладают полярными свойствами из-за наличия электронегативного атома кислорода. Каждый атом водорода в молекуле воды образует ковалентную связь с одним из атомов кислорода. При этом электроны смещаются ближе к атому кислорода, что делает молекулу воды полярной.
Когда спирт смешивается с водой, происходит взаимодействие полярных молекул обеих веществ. Они притягивают друг друга благодаря разнице в полярности. Это приводит к уменьшению объема смеси, так как молекулы воды и спирта уплотняются при взаимодействии.
В итоге, объем смеси спирта и воды становится меньше объема исходных веществ из-за их полярности и притяжения молекул друг к другу.