Адсорбция – это явление, которое происходит, когда молекулы физически или химически привязываются к поверхности твердого материала. Этот процесс широко применяется в различных областях, таких как катализ и сорбирование веществ. Понимание молекулярного механизма и особенностей адсорбции имеет большое значение для разработки новых материалов и процессов, а также для понимания фундаментальных принципов химии поверхности.
Молекулярный механизм адсорбции заключается во взаимодействии молекул с поверхностью твердого материала. Это взаимодействие может быть физическим или химическим по своей природе. Физическая адсорбция происходит из-за слабых межмолекулярных сил, таких как ван-дер-ваальсовы взаимодействия, диполь-дипольные силы и водородные связи. Химическая адсорбция, как правило, более сильная и является результатом образования химических связей между молекулами и поверхностью.
Особенности адсорбции определяются различными факторами, включая природу поверхности, свойства адсорбируемых молекул и условия окружающей среды. Поверхность может быть активной (с большим количеством активных центров) или пассивной (с небольшим количеством активных центров). Адсорбируемые молекулы могут быть поларными или неполярными, крупными или малыми. Условия окружающей среды, такие как температура и давление, также могут существенно влиять на адсорбцию.
Адсорбция: молекулярный механизм и особенности
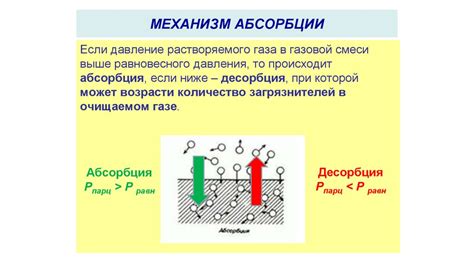
Молекулярный механизм адсорбции основан на взаимодействии молекул адсорбата с поверхностью адсорбента. Существуют различные силы, которые могут обуславливать адсорбцию, такие как ван-дер-ваальсовы силы, химическое соединение и электростатическое притяжение. Каждое из этих взаимодействий может проявляться в разной степени в зависимости от свойств поверхности и адсорбата.
Особенностью адсорбции является то, что она происходит только на поверхности адсорбента, а не в его объеме. Поэтому одно из важных свойств адсорбента - наличие достаточно большой площади поверхности. Чем больше площадь поверхности адсорбента, тем больше молекул адсорбата может быть удержано.
Кинетика адсорбции также имеет свои особенности. Существует несколько моделей, описывающих скорость адсорбции в зависимости от времени. Некоторые из этих моделей учитывают диффузию молекул адсорбата через границу раздела адсорбент-среда.
Важно отметить, что адсорбция может быть обратимым или необратимым процессом в зависимости от условий. Также, адсорбция может происходить как на гладких поверхностях, так и на пористых материалах с большой поверхностью.
- Одним из примеров адсорбции является поглощение вредных газов с поверхности активированного угля.
- Адсорбция может быть использована для удаления загрязняющих веществ из воды, например, через использование ионитов.
- В хроматографии адсорбция используется для разделения различных компонентов смеси на основе их аффинности к адсорбенту.
Таким образом, понимание молекулярного механизма и особенностей адсорбции позволяет использовать этот процесс в различных областях для разделения и очистки веществ, а также для создания эффективных каталитических систем.
Почему возникает адсорбция и как она происходит?
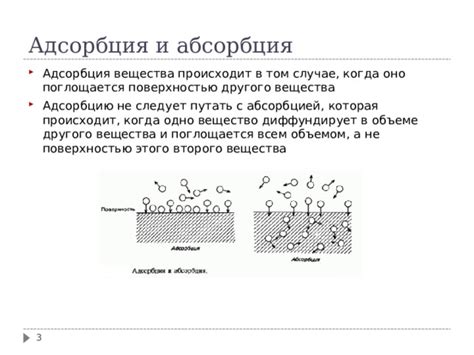
Почему возникает адсорбция? Это связано с химическими и физическими взаимодействиями между адсорбентом и адсорбатом. Например, молекулы газов могут притягиваться к поверхности адсорбента из-за диполь-дипольных взаимодействий или взаимодействий водородных связей. В случае сорбции жидкостей, причиной могут быть физические взаимодействия, такие как ван-дер-ваальсовы силы или капиллярное взаимодействие.
Как происходит адсорбция? Изначально поверхность адсорбента покрыта слоем газа или жидкости, но с приближением молекул адсорбата к поверхности, силы притяжения становятся более сильными, и молекулы начинают "прилипать" к поверхности. Этот процесс может быть обратимым или необратимым в зависимости от условий адсорбции.
Особенности адсорбции связаны с множеством факторов, таких как свойства адсорбента и адсорбата, температура и давление. Некоторые адсорбенты могут быть специфичными по отношению к определенным адсорбатам, что делает их полезными в различных процессах, таких как очистка воды или разделение смесей.
Таким образом, адсорбция возникает из-за взаимодействий между адсорбентом и адсорбатом, и происходит путем притяжения молекул адсорбата к поверхности адсорбента. Это важное явление, которое является основой для различных технологических процессов и научных исследований.
Роль молекул в процессе адсорбции
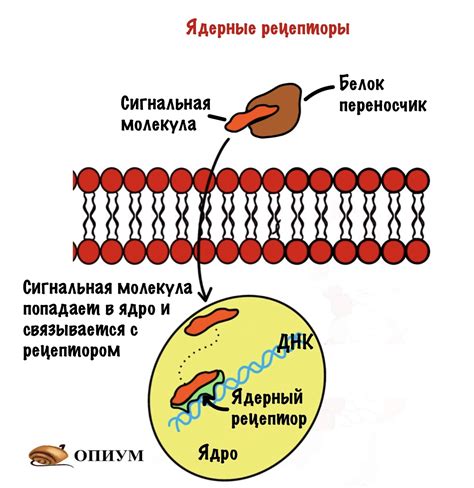
Молекулярный механизм адсорбции позволяет понять, каким образом происходит притяжение адсорбата к поверхности адсорбента. В основе этого процесса лежит взаимодействие молекул адсорбата и адсорбента.
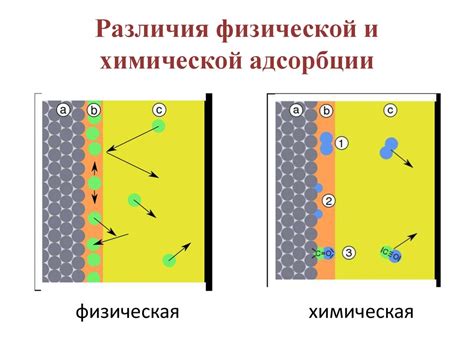
Адсорбция может быть физической или химической. В случае физической адсорбции молекулы адсорбата притягиваются к поверхности адсорбента слабыми ван-дер-Ваальсовыми силами притяжения. При этом происходит физическое взаимодействие между полярными или неполярными молекулами адсорбента и адсорбата. В случае химической адсорбции происходит образование химической связи между молекулами адсорбента и адсорбата, что делает этот процесс более значимым для реакций на поверхности.
Успешная адсорбция зависит от различных факторов, таких как температура, давление и концентрация адсорбата, а также свойства поверхности адсорбента. Специфические химические группы на поверхности адсорбента могут способствовать притяжению определенных типов молекул адсорбата.
Различные физические и химические свойства молекул также играют важную роль в процессе адсорбции. Например, молекулы с большей поверхностной площадью имеют больше возможностей для взаимодействия с поверхностью адсорбента и, следовательно, могут быть адсорбированы в больших количествах.
| Факторы, влияющие на адсорбцию | Роль молекул |
|---|---|
| Температура | Увеличение температуры обычно увеличивает кинетику адсорбции, поскольку молекулы адсорбата получают больше энергии для перемещения и удерживаются на поверхности адсорбента более слабо |
| Давление | Увеличение давления обычно увеличивает количество адсорбированных молекул, поскольку больше молекул адсорбата сталкивается и взаимодействует с поверхностью |
| Концентрация адсорбата | Увеличение концентрации адсорбата обычно увеличивает количество адсорбированных молекул, поскольку больше молекул адсорбата доступны для взаимодействия с поверхностью |
| Свойства поверхности адсорбента | Специфические химические группы на поверхности могут способствовать притяжению определенных типов молекул адсорбата |
| Физические и химические свойства молекул | Молекулы с большей поверхностной площадью имеют больше возможностей для взаимодействия с поверхностью адсорбента и могут быть адсорбированы в больших количествах |
Влияние поверхностных сил на адсорбцию
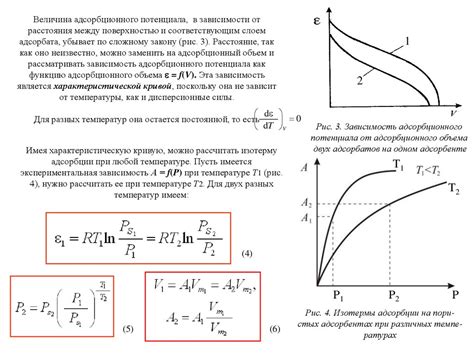
Поверхностные силы обусловлены взаимодействием между молекулами на поверхности исследуемого вещества и адсорбирующим веществом. Существуют различные типы поверхностных сил, такие как ван-дер-ваальсовы силы, электростатические силы и силы химической связи.
Ван-дер-ваальсовы силы – это слабые силы взаимодействия между атомами или молекулами, вызванные изменениями в электронном облаке. Эти силы часто являются причиной физической адсорбции. Например, при физической адсорбции газов на поверхности твердого тела, ван-дер-ваальсовы силы притяжения между атомами газа и атомами поверхности приводят к их привязке.
Электростатические силы возникают из-за разности зарядов между поверхностью и адсорбирующим веществом. Эти силы могут быть положительными или отрицательными, в зависимости от заряда и положения атомов или молекул. В некоторых случаях, электростатические силы могут приводить к химической адсорбции, когда происходит образование химической связи между адсорбирующим и адсорбируемым веществами.
Силы химической связи являются наиболее прочными и способными вызвать химическую адсорбцию. Они происходят в результате обмена электронами между адсорбирующим и адсорбируемым веществами. Такие силы могут быть вызваны, например, образованием ковалентных или ионных связей между адсорбирующими и адсорбируемыми частицами.
Влияние различных поверхностных сил на адсорбцию зависит от химической природы адсорбирующих и адсорбируемых веществ, а также от условий эксперимента. Понимание молекулярного механизма и особенностей адсорбции, связанных с поверхностными силами, является важным для разработки эффективных процессов адсорбции и применения адсорбционных материалов в различных областях науки и технологии.
Особенности адсорбции в различных условиях
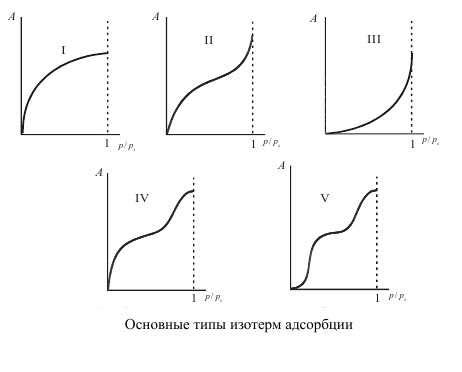
Одной из особенностей адсорбции является зависимость ее интенсивности от температуры. В большинстве случаев, с увеличением температуры, интенсивность адсорбции увеличивается. Это связано с увеличением энергии и частоты столкновений молекул, что способствует их более активному проникновению на поверхность. Однако, в некоторых случаях, адсорбция может сопровождаться этапом десорбции, при котором молекулы покидают поверхность. В этом случае, при повышении температуры, интенсивность адсорбции может снижаться.
Давление также оказывает влияние на адсорбцию. При увеличении давления, интенсивность адсорбции может возрасти благодаря увеличению числа молекул, доступных для адсорбции на поверхности. Однако, при достижении насыщения поверхности и наступлении эффекта натекания, увеличение давления может не привести к дальнейшему увеличению адсорбции.
Химическая природа вещества и поверхности также влияют на адсорбцию. Различные химические связи и силы могут приводить к разным формам адсорбции, таким как физическая или химическая адсорбция. Физическая адсорбция основана на слабых силовых взаимодействиях, таких как ван-дер-ваальсовы силы, и может быть обратимой. Химическая адсорбция является более прочной и основана на образовании химических связей между адсорбатом и адсорбентом.
Наличие или отсутствие растворителя также может влиять на адсорбцию. В растворах, молекулы адсорбата могут взаимодействовать с растворителем, что может препятствовать или, наоборот, способствовать их адсорбции на поверхность. В отсутствие растворителя, адсорбция может происходить более эффективно.
Применение адсорбции в различных отраслях науки и промышленности

В медицине адсорбция используется для очистки крови от шлаков и токсинов. Адсорбционные материалы, такие как активированный уголь и гель-сорбенты, используются для снятия отеков и устранения побочных эффектов лекарственных препаратов.
В пищевой промышленности адсорбция применяется для улучшения качества продукции. Адсорбционные материалы могут удалять нежелательные вещества из пищевых продуктов, таких как пестициды, гормоны и другие загрязнители, позволяя получить безопасную и здоровую пищу.
В экологии адсорбция широко используется для очистки воды и воздуха от различных загрязнителей. Поверхности материалов, способных к адсорбции, используются для улавливания и утилизации различных вредных веществ. Это позволяет снизить уровень загрязнения окружающей среды и сохранить природные ресурсы.
В химической промышленности адсорбция используется для разделения смесей и очистки продуктов от примесей. Адсорбционные материалы могут отделять желаемые компоненты от смеси, позволяя получить высокочистые соединения с нужными характеристиками.
В фармацевтической промышленности адсорбция применяется для получения высокочистых лекарственных препаратов. Адсорбционные материалы используются для разделения и очистки различных химических соединений, позволяя получить качественные и безопасные препараты для лечения различных заболеваний.
Таким образом, адсорбция является универсальным процессом, который находит применение во многих областях науки и промышленности. Ее молекулярный механизм и особенности делают ее неотъемлемой частью многих процессов, способствуя улучшению качества продукции, очистке окружающей среды и предоставляя возможность создания новых технологий и разработок.
Последствия и практическое значение адсорбции
Адсорбция играет важную роль в различных аспектах нашей жизни и имеет множество практических применений. Вот некоторые из них:
1. Катализаторы: Адсорбция используется для создания и улучшения катализаторов - веществ, ускоряющих химические реакции. Поверхность катализатора обычно покрыта веществами, которые способны адсорбировать реагенты, увеличивая эффективность реакций.
2. Очистка воды: Процесс адсорбции широко применяется для очистки воды от загрязнений и вредных веществ. Адсорбенты, такие как активированный уголь, могут адсорбировать органические и неорганические примеси из воды, делая ее безопасной для потребления.
3. Фармацевтика: Адсорбция используется в производстве лекарственных препаратов. Адсорбенты могут удалять вредные вещества из фармацевтических продуктов, повышая их безопасность и эффективность.
4. Хроматография: Хроматография - это метод разделения смесей веществ. Он основан на адсорбции компонентов смеси на поверхности специальных материалов. Этот метод активно применяется в химическом анализе и научных исследованиях.
5. Сорбционные системы: Адсорбция используется в сорбционных системах, таких как фильтры для очистки воздуха и газов. Адсорбенты способны адсорбировать загрязняющие вещества, снижая вредные эффекты окружающей среды.
6. Вакуумные насосы: Адсорбция играет ключевую роль в работе вакуумных насосов. Адсорбенты используются для удаления газов из закрытой системы, создавая вакуумное окружение.
Все эти примеры демонстрируют, что адсорбция имеет большое практическое значение и является неотъемлемой частью многих процессов и технологий.