Сера является одним из самых распространенных элементов на Земле и имеет большое значение как в природных процессах, так и в различных областях промышленности. Однако, несмотря на свою широкую распространенность, сера обладает рядом физических и химических особенностей, которые делают ее нерастворимой в воде.
Основной причиной нерастворимости серы в воде является ее поларность. Вода является полярным растворителем, то есть ее молекулы имеют неравномерное распределение зарядов: кислородная часть молекулы обладает отрицательным зарядом, а водородные атомы – положительным. В свою очередь, сера имеет неполярную структуру, где заряды равномерно распределены по всей молекуле.
Из-за отсутствия полярности молекулы серы не могут образовываться водородные связи с молекулами воды. Водородные связи – это силы, которые удерживают молекулы воды вместе и позволяют им образовывать решетку, что делает воду жидкой при комнатной температуре. В случае с молекулами серы, отсутствие водородных связей делает их нерастворимыми в воде и вызывает их отдельное наличие в виде кристаллов или осадка.
Причины нерастворимости серы в воде

Во-первых, основной причиной нерастворимости серы в воде является разница в полярности между этими веществами. Вода является полярным растворителем, то есть ее молекулы имеют неравномерное распределение зарядов. Это позволяет воде образовывать водородные связи и взаимодействовать с полярными молекулами других веществ. Однако сера является неполярным веществом, у нее нет заряда и молекулы серы не могут образовывать водородные связи с молекулами воды. Это препятствует их взаимодействию и растворению.
Во-вторых, сера обладает кристаллической структурой, в которой атомы серы занимают определенное положение в решетке. Это положение делает их стабильными и устойчивыми, и они не разрушаются в процессе взаимодействия с водой. Кристаллическая структура серы также обуславливает ее относительно низкую плотность и жесткость, что дополнительно затрудняет ее растворение в воде.
В-третьих, сера обладает низкой растворимостью в воде из-за низкой энтропии растворения. Растворение серы в воде сопровождается увеличением порядка молекулярной структуры вещества, что противоречит тенденции естественного движения систем к равновесию и увеличению энтропии. Поэтому процесс растворения серы в воде энергетически не выгоден и происходит с большим трудом.
Химический состав серы

Сера имеет тенденцию к образованию различных типов соединений. Однако, нерастворимость серы в воде является одной из её основных химических особенностей. В чистом состоянии сера обладает низкой растворимостью в воде – всего около 0,1 г на 100 г воды при температуре 20 ℃.
Одной из причин нерастворимости серы в воде является наличие высокоэнергетических ковалентных связей между атомами серы. Кроме того, вода – полярное растворителей, а сера – неполярное вещество. Это приводит к значительной разнице в полярности между молекулами серы и молекулами воды, что делает их слабо взаимодействующими.
Взаимодействие молекул серы с молекулами воды
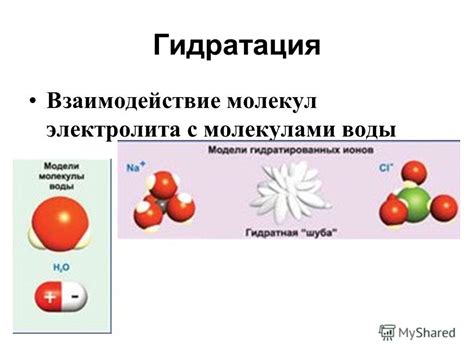
Молекулы серы образуют сетчатую структуру, в которой атомы серы связаны довольно крепко. При попытке растворить серу в воде, молекулы воды не способны разрушить эти ковалентные связи и проникнуть внутрь структуры серы.
Молекулы воды, в свою очередь, обладают полярной структурой. У них есть положительно заряженный конец (водородный атом) и отрицательно заряженный конец (кислородный атом). Полярность молекул воды приводит к тому, что они образуют водородные связи между собой.
При контакте с молекулами серы, молекулы воды образуют водородные связи только между собой, не взаимодействуя с молекулами серы.
Нерастворимость серы в воде обусловлена, таким образом, отсутствием возможности взаимодействия молекул серы с молекулами воды и подобной скоординированной сеткой ice((H2O)2...S...H2O...H2O....)).
Энергия взаимодействия между серой и водой
Однако, неполярные молекулы, такие как сера, не имеют зарядов и не образуют водородных связей с молекулами воды. В результате, энергия взаимодействия между серой и водой является недостаточной для обеспечения их химического соединения.
Энергия взаимодействия также зависит от температуры. При повышении температуры вода обладает большей кинетической энергией, что может способствовать разрушению слабых связей в сере. Однако, при комнатной температуре и нормальных давлениях энергия взаимодействия между серой и водой недостаточна для ее полного растворения.
Таким образом, нерастворимость серы в воде обусловлена энергией взаимодействия между этими веществами. Это объясняет почему сера не растворяется в воде, а образует частицы или отдельные капли.
Физические свойства серы, препятствующие ее растворению в воде

Сера является желтоватым твердым веществом с характерным запахом. Она имеет очень низкую температуру плавления (необходимо нагревать до примерно 115 градусов Цельсия) и высокую температуру кипения (находится в парообразном состоянии при примерно 444 градусах Цельсия).
Одной из главных причин нерастворимости серы в воде является ее атомная структура. Молекулы серы образуют особую кристаллическую решетку, в которой атомы связаны между собой ковалентными связями.
Ковалентные связи между серными атомами обладают очень высокой прочностью. Вода, в свою очередь, является поларной молекулой и обладает другой структурой связей. Полярность водной молекулы приводит к формированию водородных связей между молекулами воды. В результате возникают силы притяжения, препятствующие проникновению серы в воду.
Также следует отметить, что сера плохо растворима в воде из-за своей гидрофобности. Гидрофобные вещества обладают свойством не взаимодействовать с водой. В случае с серой, этот факт связан с особенностями электронной структуры ее атомов.
В целом, физические свойства серы, такие как кристаллическая структура, прочность связей и гидрофобность, являются ключевыми факторами, препятствующими ее растворению в воде.