Щелочноземельные металлы - это группа элементов периодической таблицы, состоящая из бериллия (Be), магния (Mg), кальция (Ca), стронция (Sr), бария (Ba) и радия (Ra). Их название объединяет два понятия: "щелочные" и "земельные". Почему именно такое название было дано этой группе? Все дело в их химических свойствах и месте в таблице Менделеева.
Слово "щелочные" в названии указывает на то, что щелочноземельные металлы подобны по своим химическим свойствам щелочным металлам, таким как литий, натрий и калий. Эти элементы являются очень активными и легко реагируют с водой, образуя щелочные растворы. Хотя щелочноземельные металлы не такие активные как щелочные металлы, они все же имеют сходные свойства и образуют реакции с водой и кислородом.
Слово "земельные" в названии появилось из-за того, что эти металлы являются основными компонентами земной коры. Они встречаются в природе в виде оксидов и солей, и хотя их присутствие в земле невелико, они все равно играют важную роль в многих процессах, включая рост растений и формирование геологических структур.
Таким образом, название "щелочноземельные металлы" отражает химические и геологические свойства этой группы элементов, и является описательным и понятным для химиков и геологов.
История названия щелочноземельных металлов

Название "щелочноземельные металлы" было введено в науку русским химиком А. П. Павловым в начале XIX века. Эти металлы получили такое название из-за своих свойств и химических реакций, которые они могут совершать.
Первый элемент этой группы, кальций, был известен с древних времен. Еще в Древнем Египте использовали известняк, содержащий кальций, для создания различных многофункциональных материалов. Однако, только в 1808 году французский химик Гай-Луссак и английский химик Хамфри Дэви разработали метод изоляции кальция.
Следующий металл в группе – бериллий – был открыт в 1798 году немецким химиком К. В. Вильгельмом. Изначально он назвал новый элемент глюкумием, но позже его решили назвать бериллием.Это название было дано в честь минерала «берилл», который содержит этот металл.
Магний, третий элемент группы, был открыт в 1808 году французским химиком Сиром Антуаном. Он изолировал металлическую форму магния из оксида магния при помощи электролиза. Название "магний" образовалось от слова "магнит", так как этот металл обладает подобными свойствами.
Следующим элементом в группе щелочноземельных металлов является кальций. Широкое применение кальция в различных отраслях промышленности привело к его изучению множеством ученых. Используя разные методы, такие как водород-кальциевый метод и электролиз, химики смогли получить чистый кальций.
Последний элемент группы – радий – был открыт в начале XX века мадам Кюри. Она открыла радий вместе с полонием. Радий получил свое название от латинского слова "radius", что означает "луч", в связи со своей радиоактивностью и ярким излучением.
Таким образом, история названия щелочноземельных металлов связана с их свойствами, историческими источниками и вкладом ученых в открытие и исследование этих элементов.
Происхождение слова "щелочноземельные"

Термин "щелочноземельные" происходит от сочетания двух слов: "щелочь" и "земля".
Слово "щелочь" в русском языке обозначает сильную щелочь, то есть вещество с высоким уровнем pH, которое оказывает щелочное действие. Щелочи широко используются в различных сферах, таких как химия, медицина и промышленность.
Слово "земля" в данном контексте означает минералы, которые были найдены в почве. Щелочноземельные металлы обладают химическими свойствами, характерными для минералов в земле.
Таким образом, название "щелочноземельные металлы" отражает химические свойства данных элементов, которые похожи на свойства щелочей и материалов, найденных в земле.
Интересно отметить, что термин "щелочноземельные" применяется еще с XIX века и был предложен известным немецким химиком Хайнрихом Розе. Он выделил эту группу элементов, так как они обладают общими химическими свойствами и образуют щелочные оксиды и гидроксиды.
Таким образом, название "щелочноземельные металлы" имеет свою историю и основано на химических свойствах данных элементов.
| Название элемента | Символ |
|---|---|
| Бериллий | Be |
| Магний | Mg |
| Кальций | Ca |
| Стронций | Sr |
| Барий | Ba |
| Радий | Ra |
Обнаружение щелочноземельных металлов

Щелочноземельные металлы были открыты и обнаружены в разное время и различными учеными. Каждый металл из этой группы имеет некоторые уникальные свойства, что позволяет их легко обнаружить и идентифицировать.
Первый щелочноземельный металл, кальций, был открыт в 1808 году с помощью электролиза ртути оксида кальция. Этот эксперимент был проведен самим Сэром Хамфри Дэви. С того времени было возможно выбирать кальций из своей окружающей среды.
Следующий металл, бериллий, был обнаружен в 1797 году французским химиком Луи-Николасом Ваукленом. Он использовал электролитический метод для получения бериллия из хлорида бериллия. Вауклен смог изолировать этот металл и исследовать его свойства.
Магний, еще один щелочноземельный металл, был открыт в 1755 году шведским химиком Химитом Кремером. Он изолировал магний из соляной кислоты и определил его химические свойства.
Ряд щелочноземельных металлов продолжает расширяться с появлением новых элементов. Каждый новый металл обнаруживается при помощи различных химических и физических методов, включая спектроскопию и рентгеновскую дифракцию. Это позволяет ученым точно определить свойства и химическую реактивность новых элементов щелочноземельных металлов.
| Элемент | Год открытия | Открыватель |
|---|---|---|
| Кальций | 1808 | Сэр Хамфри Дэви |
| Бериллий | 1797 | Луи-Николас Вауклен |
| Магний | 1755 | Химит Кремер |
Физические свойства щелочноземельных металлов

Физические свойства щелочноземельных металлов можно описать следующим образом:
1. Металлический блеск: Щелочноземельные металлы имеют характерный блеск на свежем воздухе. Они являются отличными проводниками тепла и электричества.
2. Мягкость: Бериллий – самый твёрдый из щелочноземельных металлов, но остальные элементы этой группы являются мягкими металлами, которые можно нарезать ножом или смять руками.
3. Низкое плотность: Щелочноземельные металлы обладают низкой плотностью. Исключением является бериллий, который имеет высокую плотность.
4. Химическая активность: Щелочноземельные металлы реагируют с водой, но они менее реактивны, чем щелочные металлы. Они легко окисляются на воздухе, образуя защитную плёнку оксида на поверхности.
5. Электроотрицательность: Щелочноземельные металлы обладают низкой электроотрицательностью, что делает их хорошими веществами для формирования ионов с положительным зарядом.
6. Амфотерность: Один из наиболее интересных фактов о щелочноземельных металлах заключается в их амфотерности. Это означает, что они проявляют свойства как металлов, так и неметаллов. Например, оксиды щелочноземельных металлов могут реагировать как со сильными кислотами, так и со слабыми основаниями.
Изучение физических свойств щелочноземельных металлов имеет широкий спектр практических применений, включая разработку новых материалов, изготовление легких сплавов, создание лекарственных препаратов и различные промышленные процессы.
Химические свойства щелочноземельных металлов

Первое химическое свойство щелочноземельных металлов - их способность образовывать ионные соединения с отрицательно заряженными ионами. Это связано с их электроотрицательностью и способностью отдавать два электрона для стабилизации своей электронной оболочки. Благодаря этому, щелочноземельные металлы образуют стабильные соединения с кислородом (оксиды), серой (сульфиды) и другими неметаллами.
Второе химическое свойство щелочноземельных металлов - их реакционная способность с водой. Хотя они не так активны, как щелочные металлы, щелочноземельные металлы все равно реагируют с водой, образуя гидроксиды и высвобождая водород. Например, магний и вода взаимодействуют, образуя гидроксид магния и выделяя водородный газ:
Mg + 2H2O → Mg(OH)2 + H2
Третье химическое свойство щелочноземельных металлов - их способность образовывать соли с различными кислотами. Например, кальций может образовывать соли с азотной кислотой, образуя нитрат кальция:
Ca + 2HNO3 → Ca(NO3)2 + H2
Кроме того, щелочноземельные металлы обладают высокой теплопроводностью, электропроводностью и плотностью. Они также способны образовывать сплавы с другими металлами, что дает им широкий спектр применения в промышленности и технологии.
В целом, химические свойства щелочноземельных металлов делают их важными для многих процессов и приложений, от производства лекарств до производства сплавов и батарей. Изучение их химических свойств позволяет лучше понять и использовать эти элементы в нашей повседневной жизни.
Применение щелочноземельных металлов

Щелочноземельные металлы, такие как магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra), обладают разнообразными свойствами и находят широкое применение в различных отраслях промышленности и научных исследованиях.
Магний (Mg) является одним из самых легких металлов и используется преимущественно в авиационной и автомобильной промышленности. Он используется для производства легких сплавов, которые обеспечивают повышенную прочность и стойкость к коррозии. Магний также используется в производстве белых светодиодов, пиротехнических смесей и лекарственных препаратов.
Кальций (Ca) широко применяется в строительной отрасли для производства строительных материалов, таких как цемент, известь и гипс. Он также используется в процессе осаждения металлов, в производстве сплавов и в производстве сталей. Кальций имеет важное значение для здоровья человека и животных, так как является важным элементом в составе костей и зубов.
Стронций (Sr) используется в производстве пиротехнических материалов и светофильтров для телевизоров и компьютерных мониторов. Он также применяется в медицине для диагностики болезней с помощью радиоактивных изотопов стронция.
Барий (Ba) используется в производстве светоотражающих покрытий, стекловолокна и телевизионных экранов. Барий-содержащие соединения также используются в пиротехнике и в медицине для рентгенологических исследований.
Радий (Ra) является редким и радиоактивным металлом. Его радиоактивные свойства позволяют использовать его в научных исследованиях, включая исследование радиоактивности и радиоизотопов. Ранее радий использовался в производстве светящихся часов и часов, но из-за его высокой токсичности его применение было ограничено.
Щелочноземельные металлы имеют важное значение в различных отраслях промышленности и науке и продолжают привлекать внимание исследователей и инженеров для разработки новых применений и улучшения существующих технологий.
Влияние щелочноземельных металлов на окружающую среду

Щелочноземельные металлы, включающие в себя бериллий, магний, кальций, стронций, барий и радий, играют важную роль в нашей жизни, однако их воздействие на окружающую среду также должно быть учтено.
Одним из главных источников загрязнения окружающей среды щелочноземельными металлами является промышленность, особенно металлургический и химический секторы. В ходе процессов добычи, производства и утилизации этих металлов может выделяться значительное количество отходов и выбросов, которые могут негативно сказываться на качестве воздуха, воды и почвы.
Бериллий, например, широко используется в аэрокосмической и оборонной промышленности, а также в производстве электронной техники. Однако он является токсичным и может вызывать серьезные здоровые проблемы у людей, которые сталкиваются с ним в процессе работы или проживания рядом с предприятиями, где добывается или используется бериллий. Магний, хотя и не является токсичным, но его выбросы в атмосферу могут приводить к образованию смога. Кальций, стронций и барий также могут быть вредными при попадании в окружающую среду в больших количествах.
Однако, несмотря на потенциальные опасности, существуют технологии и методы, которые позволяют снизить негативное воздействие щелочноземельных металлов на окружающую среду. Это включает разработку и использование более эффективных систем очистки выбросов, контрольные механизмы для ограничения выбросов в окружающую среду, а также утилизацию и переработку отходов.
В целом, влияние щелочноземельных металлов на окружающую среду должно быть тщательно изучено и учтено при разработке и применении этих металлов в различных сферах промышленности. Только так можно обеспечить устойчивое и экологически безопасное использование этих важных ресурсов.
Значимость щелочноземельных металлов для научных исследований
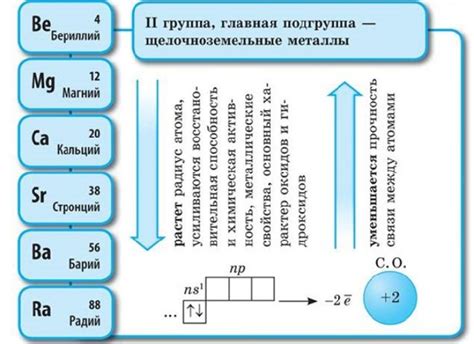
Эти металлы играют важную роль в научных исследованиях благодаря своим уникальным химическим свойствам:
1. Важность для биологии и медицины. Магний, кальций и барий являются необходимыми элементами для многих биологических процессов в организмах живых существ. Они участвуют в работе мышц и нервов, регулируют основные физиологические функции, укрепляют зубы и кости. Бериллий и стронций также находят применение в медицине, например, в радиологии и терапии опухолей.
2. Использование в энергетике. Бериллий находит применение в ядерной энергетике, где используется в конструкции ядерных реакторов. Это металл обладает высокой степенью прозрачности для нейтронов, что позволяет контролировать деление ядер и производить радиационные измерения.
3. Участие в процессах катализа. Бериллий и магний являются важными катализаторами в различных химических реакциях. Они ускоряют скорость реакции и снижают энергию активации, что делает процессы более эффективными и экономически выгодными.
Таким образом, щелочноземельные металлы представляют собой группу элементов, которые играют значимую роль в различных научных исследованиях. Их химические свойства и уникальные способности открывают новые перспективы и возможности в биологии, медицине, энергетике и других областях науки.