Вода – это одна из наиболее распространенных и важных жидкостей на Земле. Мы ежедневно используем ее во многих сферах жизни, от питья до ухода за телом. Но почему вода именно жидкость? Давайте разберемся.
Молекулы воды состоят из двух атомов водорода и одного атома кислорода, что делает ее молекулу поларной. Вода обладает дипольным свойством, то есть разделена на положительно заряженную сторону, где находятся атомы водорода, и отрицательно заряженную сторону, где находится атом кислорода. Это положение вызывает различные взаимодействия между молекулами воды.
Когда вода находится в жидком состоянии, молекулы взаимодействуют друг с другом с помощью межмолекулярных сил. У положительной стороны одной молекулы воды есть притяжение к отрицательной стороне другой молекулы. Это силы взаимодействия, называемые водородными связями, которые делают воду жидкостью.
Свойства и состав воды: научное объяснение

В составе воды молекула воды, или H2O, имеет простую структуру: два атома водорода, соединенные с атомом кислорода при помощи ковалентных химических связей. Эта структура обеспечивает воде ее основные свойства.
| Свойство | Объяснение |
|---|---|
| Полярность | Молекула воды имеет полярную структуру, что означает, что она имеет заряды различной полярности. Это позволяет водным молекулам образовывать водородные связи, что делает воду уникальной. |
| Высокая теплоемкость | Вода обладает способностью поглощать и отдавать большое количество тепла, что делает ее эффективным теплоносителем и помогает поддерживать стабильную температуру на Земле. |
| Высокое поверхностное натяжение | Молекулы воды взаимодействуют друг с другом, образуя тонкую пленку на поверхности воды. Это позволяет некоторым организмам перемещаться по поверхности воды. |
| Высокая способность растворять вещества | Вода является универсальным растворителем, так как у ее молекул есть заряженные участки. Это позволяет различным веществам растворяться в воде и выполнять функции в организмах. |
| Высокая плотность в жидком состоянии | Вода имеет наибольшую плотность при температуре 4 градуса Цельсия. Это позволяет ей оставаться жидкостью в широком диапазоне температур, что важно для жизни. |
Знание свойств и состава воды позволяет лучше понять ее роль в природных и биологических процессах. Эта уникальная жидкость играет ключевую роль в жизни на Земле и продолжает удивлять ученых своими необычными свойствами.
Структура молекулы воды: ключевой фактор
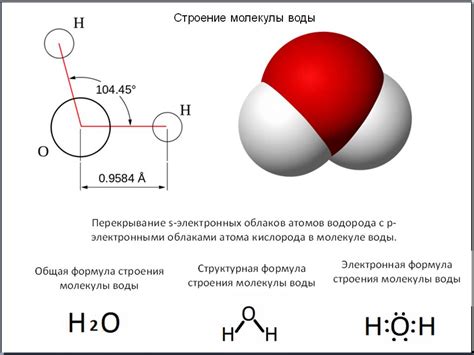
Структура молекулы воды играет ключевую роль в ее свойствах и состоянии. Молекула воды состоит из двух атомов водорода и одного атома кислорода, соединенных ковалентной связью.
Уникальной особенностью структуры молекулы воды является ее полярность. Атом кислорода в молекуле воды имеет высокую электроотрицательность, что делает эту часть молекулы частично отрицательно заряженной, в то время как атомы водорода будут частично положительно заряженными. Это неравномерное распределение заряда создает положительную и отрицательную полярные характеристики внутри молекулы воды.
Полярность молекулы воды позволяет ей проявлять межмолекулярные силы, известные как водородные связи. Водородные связи возникают благодаря притяжению положительно заряженного атома водорода одной молекулы к отрицательно заряженному атому кислорода соседней молекулы. Эти слабые связи позволяют молекулам воды взаимодействовать и образовывать структуры, называемые кластерами. Благодаря водородным связям, молекулы воды организуются в решетку или сетку.
Структура кластеров и их сетки предоставляет молекулам воды возможность двигаться и соприкасаться друг с другом. Из-за способности молекул воды образовывать водородные связи, они образуют более жесткую структуру, чем многие другие жидкости. Эта особенность делает воду очень плотной и придает ей свои характерные физические свойства, такие как высокая теплопроводность, поверхностное натяжение и высокая температура кипения.
Структура молекулы воды также объясняет ее летучесть и растворительные способности. Благодаря водородным связям, молекулы воды могут легко притягивать и вступать во взаимодействие с другими молекулами, что делает воду хорошим растворителем для многих веществ.
Взаимодействие между молекулами: причина жидкостного состояния
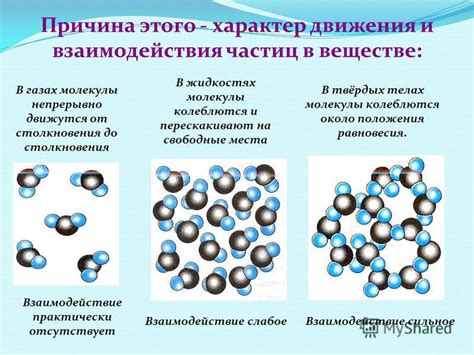
Водородная связь – это сильное притяжение между атомом водорода одной молекулы и электроотрицательным атомом (кислородом или азотом) другой молекулы. В случае с водой, каждая молекула воды может образовывать до четырех водородных связей – две соседние молекулы связываются между собой двумя связями, а сама молекула может образовывать еще две связи с другими молекулами воды.
Эти водородные связи обуславливают множество свойств воды, в том числе и ее жидкостное состояние. Каждая водородная связь является слабой по отдельности, однако их множество взаимодействует силой, достаточной для создания и поддержания формы и объема жидкости.
Кроме водородных связей, молекулы воды также проявляют дипольные моменты. Дипольный момент возникает из-за различия в электронной плотности между атомом кислорода и атомами водорода. Эти дипольные моменты взаимодействуют друг с другом, удерживая молекулы воды вместе и являются дополнительным фактором, способствующим жидкостному состоянию воды.
Водородные связи и дипольные моменты создают слабые силы притяжения между молекулами воды, что делает ее жидкостью при комнатной температуре и давлении. В то же время, эти силы не настолько сильны, чтобы молекулы были неподвижными, что позволяет воде сохранять свою подвижность и текучесть.
Таким образом, взаимодействие между молекулами воды, обусловленное водородными связями и дипольными моментами, является основной причиной жидкостного состояния воды.
Температурный диапазон и плотность: важные характеристики

Интересно, что вода имеет наибольшую плотность при температуре 4°C (39°F). Это означает, что при данной температуре вода достигает наивысшей плотности, а температуры выше или ниже вызывают увеличение объема и, соответственно, уменьшение плотности.
Это важно для живых организмов, так как нижележащие слои воды остаются более холодными, а верхние слои поддерживают более теплую температуру. Этот процесс называется конвекцией и позволяет поддерживать устойчивую температуру воды и обеспечивает условия для жизни разнообразных организмов, находящихся в водных экосистемах.
Благодаря способности воды изменять свою плотность в зависимости от температуры, она также обладает уникальными свойствами, такими как плавание льда на поверхности воды. На поверхности воды образуется лед, который имеет меньшую плотность, чем вода, что позволяет ему плавать. Это явление очень важно для биологических систем, так как защищает водоемы от полного замерзания и сохраняет тепло в нижележащих слоях.
Таким образом, температурный диапазон и плотность воды играют важную роль в поддержании устойчивости жидкой среды и поддержании жизни на планете.