Жирные кислоты - это одна из самых важных групп органических соединений, которые играют фундаментальную роль в биохимических процессах организма. Необычное название этих веществ связано с их структурой и свойствами.
Высшие карбоновые кислоты отличаются наличием длинной углеродной цепи, состоящей из прямых атомов углерода, атомов водорода и одного атома кислорода, прикрепленного к концу цепи. Из-за этой структуры, карбоновые кислоты мягкой консистенции напоминают вещества, похожие на жиры. Поэтому они и названы "жирными".
Слово "жирный" тесно связано с понятием "жир". Жировые кислоты содержатся в жирах животных и растительных маслах. Эти вещества играют важную роль в клеточном метаболизме, синтезе стероидов, энергетическом обмене и других процессах организма. Главным образом, жирные кислоты служат "строительными блоками" жиров, которые являются важным источником энергии для организма.
Что такое высшие карбоновые кислоты
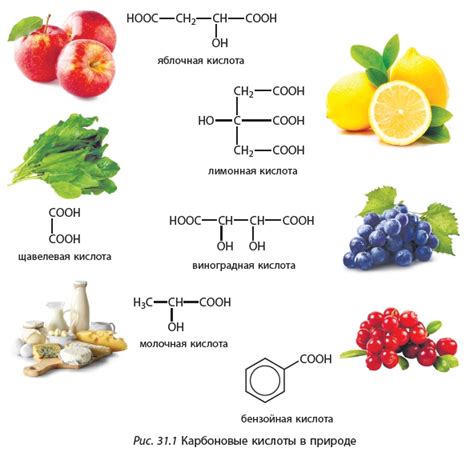
Высшие карбоновые кислоты представляют собой класс органических соединений, состоящих из длинной цепи углеродных атомов, на одном из которых находится функциональная группа карбоксильной кислоты. Обычно длина углеродной цепи в высших карбоновых кислотах колеблется от 12 до 24 атомов.
Высшие карбоновые кислоты получили название "жирные" из-за того, что большинство из них образуют жирные вещества, такие как жиры и масла. Эти соединения являются главными компонентами структуры жиров и имеют важное значение для функционирования организма.
Одной из основных характеристик высших карбоновых кислот является их гидрофобность, то есть нежелание взаимодействовать с водой. Это связано с тем, что углеродные цепи карбоновых кислот содержат много атомов углерода, которые образуют гидрофобные хвосты.
Высшие карбоновые кислоты часто используются в качестве сырья для производства моющих средств, косметических и фармацевтических продуктов, пищевых добавок и других полезных веществ. Они имеют широкий спектр применения и являются важными компонентами в различных отраслях промышленности.
| Примеры высших карбоновых кислот: | Углеродная цепь: | Название: |
| Миристиновая кислота | C14H28COOH | Тетрадециловая кислота |
| Пальмитиновая кислота | C16H32COOH | Гексадециловая кислота |
| Стеариновая кислота | C18H36COOH | Октадециловая кислота |
| Линолевая кислота | C18H32O2 | Октадециловая кислота |
Зачем называют жирными

Высшие карбоновые кислоты, состоящие из длинных углеводородных цепей, называют жирными по нескольким причинам.
Во-первых, жирные кислоты широко распространены в жирах и маслах, которые являются основным источником этих соединений. Жиры, как известно, имеют высокую энергетическую ценность и служат запасным пищевым веществом для организма. Поэтому кислоты, образующие жиры, получили название "жирные" для удобства и отражения их пищевой ценности.
Во-вторых, жирные кислоты обладают гидрофобными свойствами и слаборастворимы в воде, в отличие от карбоновых кислот с короткими углеводородными цепями. Этот факт делает их прекрасными материалами для строительства липидных мембран, которые являются основой клеточной структуры. Название "жирные" указывает на гидрофобность этих соединений и их роль в формировании липидных мембран.
Таким образом, название "жирные" не только отражает пищевую ценность и энергетическую ценность высших карбоновых кислот, но и указывает на их свойства, которые играют важную роль в клеточных процессах и биологических структурах.
Размер молекул
Карбоновые кислоты сравнительно длинные молекулы, состоящие из химически связанных углеродных атомов и атомов кислорода. При увеличении числа углеродных и атомов, общая длина молекулы также увеличивается. Более длинные молекулы имеют больше места для взаимодействия между молекулами, в результате чего они имеют более сильные межмолекулярные силы притяжения.
Эти силы притяжения могут приводить к тому, что карбоновые кислоты с более длинными молекулами имеют более высокую температуру плавления и кипения по сравнению с карбоновыми кислотами с более короткими молекулами. В результате, карбоновые кислоты с более длинными молекулами могут иметь более плотную и твердую структуру, что обычно связывается с "жирностью" этих кислот.
Таким образом, размер молекулы влияет на свойства карбоновых кислот и объясняет, почему более длинные молекулы воспринимаются как "жирные".
Отличие от низших карбоновых кислот
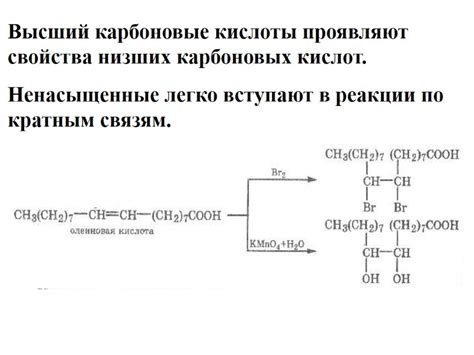
Высшие карбоновые кислоты, известные также как жирные кислоты, имеют несколько отличительных особенностей по сравнению с низшими карбоновыми кислотами.
Одно из основных отличий заключается в длине углеводородной цепи у высших карбоновых кислот. У них содержатся от 8 до 24 атомов углерода, в то время как низшие карбоновые кислоты обычно имеют менее 6 атомов углерода.
Также важно отметить, что высшие карбоновые кислоты имеют более высокие температуры плавления и кипения по сравнению с низшими карбоновыми кислотами. Это связано с увеличением размера молекул, что делает их более сложными и стабильными соединениями.
Жирные кислоты также часто обладают гидрофобными свойствами, то есть плохо смешиваются с водой. Это объясняется наличием в их молекулах длинной гидрофобной углеводородной цепи. В связи с этим, высшие карбоновые кислоты подходят для использования в липидных системах, таких как жиры и масла.
Поскольку высшие карбоновые кислоты обладают большей молекулярной массой, они имеют более низкую растворимость в воде по сравнению с низшими карбоновыми кислотами. Это свойство делает их полезными в качестве компонентов веществ, используемых для разделения или извлечения соединений в химической или фармацевтической промышленности.
Почему именно "жирные"

Термин "жирные" применяется к высшим карбоновым кислотам из-за их физических свойств и растительного происхождения. Эти кислоты обладают высокой молекулярной массой и обычно имеют густую, маслянистую или жирную структуру. Они также широко распространены в жирах и маслах, которые служат основным энергетическим и структурным компонентами живых организмов.
Карбоновые кислоты также получили название "жирные" из-за своей способности образовывать жировые кислоты, которые являются важной составляющей жира. Жировые кислоты являются ключевыми компонентами клеточных мембран и играют важную роль в обмене веществ, предоставляя энергию и поддерживая здоровье организма.
Таким образом, термин "жирные" стал общепринятой идиомой для обозначения высших карбоновых кислот, отражая их природу, свойства и широкое присутствие в жирах и маслах.
Физические свойства
Высшие карбоновые кислоты, такие как олеиновая кислота, пальмитиновая кислота и стеариновая кислота, широко известны своим жирным видом и характерными физическими свойствами.
Одним из основных физических свойств высших карбоновых кислот является их высокая вязкость и пластичность при обычных температурах коллекции. Это свойство делает их подходящими для использования в производстве масел, жиров и мыла. Благодаря высоким значениям температуры плавления, которые составляют около 40-70°С в зависимости от конкретного карбонового числа, высшие карбоновые кислоты обладают высокой стабильностью при нормальных условиях.
Еще одной важной физической характеристикой жирных кислот является их низкая растворимость в воде. Благодаря этому свойству жирные кислоты могут быть использованы в качестве гидрофобных поверхностно-активных веществ, которые способны образовывать плотные слои на поверхности воды.
Жирные кислоты также обладают способностью образовывать межмолекулярные водородные связи, что влияет на их кристаллическую структуру. Благодаря этому свойству, жирные кислоты могут образовывать кристаллические структуры разной формы и размера, что играет важную роль в их использовании в производстве пищевых продуктов и химических соединений.
Таким образом, высшие карбоновые кислоты, известные как жирные кислоты, обладают уникальными физическими свойствами, которые делают их ценными в различных областях промышленности и науки.
Температурные характеристики
Высшие карбоновые кислоты получили свое название «жирные» из-за их способности быть жидкими или твердыми веществами при комнатной температуре. Это происходит из-за длины углеродной цепи, которая составляет основу молекулы кислоты.
Чем длиннее цепь углерода, тем выше температура, при которой кислота остается жидкой. Например, уксусная кислота (CH3COOH), состоящая только из двух углеродных атомов, является жидкой при комнатной температуре. Однако, стеариновая кислота (C17H35COOH), содержащая семнадцать углеродных атомов, является твердым веществом.
Этот феномен объясняется силами взаимодействия между молекулами кислоты. Чем длиннее углеродная цепь, тем больше взаимодействий между молекулами и тем выше температура, при которой кислота переходит в твердое состояние. Обратный эффект также существует: карбоновые кислоты с малым количеством углеродных атомов обычно остаются в жидком состоянии.
| Карбоновая кислота | Формула | Температура плавления (°C) |
|---|---|---|
| Уксусная кислота | CH3COOH | 16.6 |
| Стеариновая кислота | C17H35COOH | 69 |
| Пальмитиновая кислота | C15H31COOH | 63.1 |
Таблица показывает разницу в температуре плавления между различными высшими карбоновыми кислотами. С каждым дополнительным углеродным атомом в цепи кислоты, температура плавления обычно увеличивается. Это делает более длинные карбоновые кислоты полезными в качестве компонентов для твердых жиров и масел, так как они способны формировать структуру и придавать твердость продуктам при комнатной температуре.
Гидрофобность

Молекулы жирных кислот состоят из длинной гидрофобной углеводородной цепи, называемой хвостом, и гидрофильной карбоксильной группы, называемой головкой. Хвост, состоящий из множества углеродных и водородных атомов, обладает высокой электроотрицательностью, что делает его неполярным и нерастворимым в воде.
Из-за этой гидрофобной природы жирные кислоты плохо смешиваются с водой и формируют маслянистые капли или слои на поверхности воды. Они также способны образовывать мицеллы, структуры, в которых гидрофобные хвосты смотрят в одну сторону, обращенную от воды, а гидрофильные головки ориентированы к воде.
Гидрофобность высших карбоновых кислот влияет на их растворимость, поведение вещества в различных окружающих средах и выполняемые ими функции в организме. Например, жирные кислоты являются основными компонентами жиров в организме, обеспечивающими энергию и структурную поддержку клеток.
Химические свойства

Высшие карбоновые кислоты также обладают растворяющими свойствами, что позволяет им хорошо смешиваться с многими органическими растворителями, такими как этиловый спирт или ацетон. Это делает карбоновые кислоты важными компонентами в производстве различных химических соединений и материалов.
Кроме того, высшие карбоновые кислоты обладают относительно высокой кислотностью, что связано с их структурой и наличием карбоксильной группы (-COOH). Именно благодаря этой особенности жирные кислоты могут участвовать в реакциях с щелочами, металлами и другими веществами, образуя различные продукты в химических процессах.
Реакции окисления
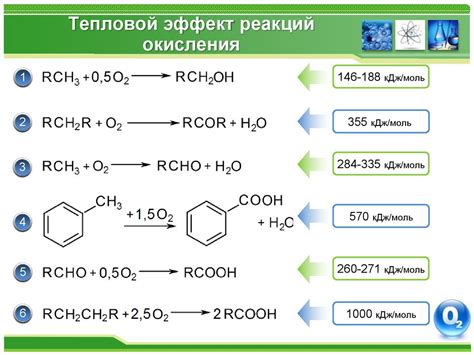
В высших карбоновых кислотах процесс окисления играет важную роль и приводит к образованию жирных соединений. Реакция окисления происходит при взаимодействии с кислородом из воздуха или с другими окислителями.
Окисление карбоновых кислот может привести к образованию различных продуктов, включая альдегиды, кетоны, спирты и карбоновую кислоту более высокого порядка. Например, окисление уксусной кислоты может привести к образованию уксусного альдегида, который имеет яркий аромат и широко используется в пищевой промышленности.
Реакция окисления высших карбоновых кислот обычно требует наличия катализатора или повышенной температуры. Такие реакции могут происходить в организмах живых существ, а также в промышленности при производстве различных продуктов, включая масла, жиры и мыло.
Реакции окисления являются важным процессом, который позволяет использовать высшие карбоновые кислоты для синтеза различных соединений и получения необходимых продуктов. Благодаря этим реакциям мы можем получать различные жиры, которые широко применяются в пищевой, химической и косметической промышленности.