Атом - одно из основных понятий в физике и химии, описывающее строение вещества. Ключевым элементом атома является его ядро, которое содержит протоны и нейтроны. Интересно, что заряд ядра атома всегда положительный, и это не является случайностью.
Позитивный заряд ядра атома обусловлен наличием протонов - элементарных частиц со стабильным положительным зарядом. Такое строение ядра является следствием взаимодействия протонов друг с другом и их силовым взаимодействием с нейтронами. Огромное притяжение протонов обеспечивается силой ядерного взаимодействия, которая поддерживает их внутри ядра.
Важно отметить, что в каждом атоме количество протонов всегда равно количеству электронов, за исключением ионов, которые имеют различное количество зарядовых элементарных частиц. Такая несбалансированность зарядов невозможна в обычных атомах, так как они являются электрически нейтральными. То есть, количество положительного заряда протонов в ядре равно количеству отрицательного заряда электронов, образующих оболочку вокруг ядра.
Почему заряд ядра положительный?
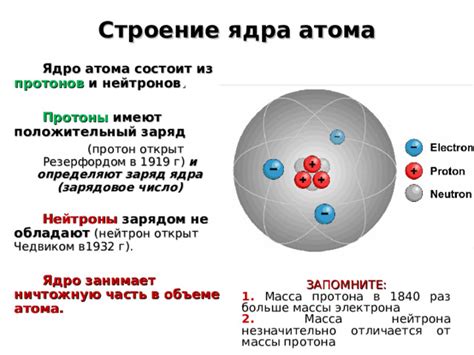
Протоны имеют положительный электрический заряд, равный элементарному заряду, и несут на себе единичный заряд. Заряд протонов и их количество в ядре определяются элементарными физическими константами, такими, как элементарный заряд и константа Планка.
Положительный заряд ядра обусловлен электромагнитными взаимодействиями между протонами внутри него. Протоны имеют одинаковый заряд, поэтому их взаимодействие приводит к образованию положительного заряда в ядре.
Отрицательный заряд в атоме представлен электронами, которые вращаются вокруг ядра по электронным оболочкам. Электроны имеют отрицательный заряд, также равный элементарному заряду. Таким образом, положительный заряд ядра балансируется отрицательным зарядом электронов, что делает атом электрически нейтральным.
Важно отметить, что в некоторых случаях, например, при наличии радиоактивных изотопов, ядра атомов могут иметь и отрицательный заряд. Это связано с присутствием в них избытка электронов или недостатком протонов.
Структура атома и заряд ядра
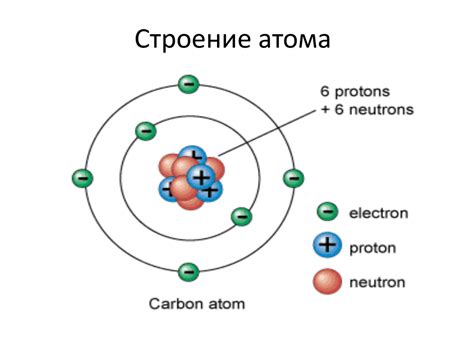
Одной из ключевых характеристик ядра является его заряд. Заряд ядра всегда положительный, так как оно содержит протоны – частицы с положительным электрическим зарядом. Нейтроны, в свою очередь, не имеют электрического заряда и не влияют на общий заряд ядра.
Заряд ядра создает электрическое поле вокруг него, которое обеспечивает притяжение электронов к ядру. Электроны, обладающие отрицательным зарядом, равновесно распределяются по электронным оболочкам, образуя структуру атома. Благодаря силе электростатического притяжения электроны не падают на ядро и образуют устойчивую атомную структуру.
Положительный заряд ядра и отрицательный заряд электронов компенсируют друг друга и делают атом электрически нейтральным. Это позволяет атомам образовывать связи между собой и образовывать структуры, которые составляют все материалы, которые мы видим в окружающем мире.
Влияние притяжения на заряд ядра
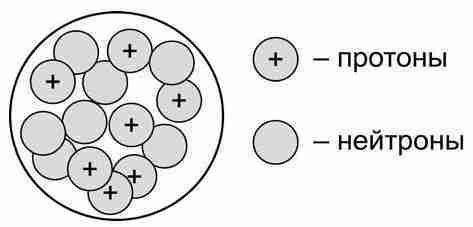
Заряд ядра атома всегда положительный из-за влияния притяжения на его составляющие частицы.
В атоме присутствуют нейтроны и протоны, которые образуют ядро. Протоны имеют положительный заряд, а нейтроны не имеют заряда. Электроны, находящиеся на орбиталях вокруг ядра, имеют отрицательный заряд. Таким образом, атом остается электрически нейтральным как сумма положительного заряда ядра и отрицательного заряда электронов.
Положительный заряд ядра обусловлен притяжением протонов друг к другу. Протоны являются заряженными частицами и, по закону электростатики, заряды одинакового знака отталкиваются, а заряды разных знаков притягиваются. В ядре атома протоны притягиваются друг к другу силой, преодолевающей электрическую отталкивающую силу. Это притяжение создает силу, удерживающую протоны вместе в ядре.
| Заряд | Силы, обусловливающие заряд |
|---|---|
| Положительный заряд ядра | Притяжение протонов друг к другу |
| Отрицательный заряд электронов | Притяжение электронов к ядру |
Именно благодаря притяжению протонов ядро атома приобретает положительный заряд. Этот заряд создает электростатическое поле, которое влияет на поведение электронов в атоме. Взаимодействие между зарядами в атоме обеспечивает его структуру и свойства.