Взгляните вокруг – вы окружены твердыми телами и жидкостями, которые не дезинтегрируются на молекулы. Но почему так происходит? Что делает эти вещества такими стойкими и устойчивыми?
Ответ кроется в строении и взаимодействии молекул. Вживую посмотрите на предмет перед собой – это может быть книга, кубик льда или стакан с водой. В каждом из этих объектов молекулы взаимодействуют друг с другом и находятся в определенном порядке.
Твердые тела характеризуются плотным расположением молекул, которые образуют регулярную структуру. Молекулы твердых тел взаимодействуют электромагнитными силами, образуя кристаллическую решетку. Эти взаимодействия обеспечивают жесткость и устойчивость твердых тел. Независимо от сил, действующих на них, молекулы твердых тел сохраняют свою структуру и не разрушаются на молекулярном уровне.
Жидкости же характеризуются более свободным движением молекул. В отличие от твердых тел, молекулы жидкостей находятся ближе друг к другу, но у них позволено слегка менять свое положение. Молекулы жидкости взаимодействуют слабее, чем молекулы твердых тел, что позволяет им двигаться и принимать форму сосуда, в котором находятся.
Молекулярная структура вещества
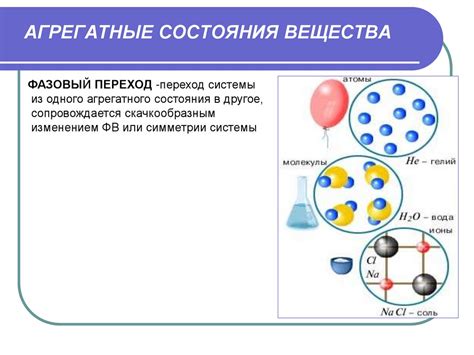
Молекулярная структура вещества определяет его физические и химические свойства. Она описывает, из каких молекул состоит вещество и как они взаимодействуют друг с другом.
В случае жидкостей и твердых тел молекулы обладают определенной степенью упорядоченности. В жидкости молекулы располагаются близко друг к другу, но не имеют фиксированной позиции. Они способны перемещаться и изменять свою структуру под влиянием внешних условий.
В твердом теле молекулы, наоборот, организованы в более жесткую, упорядоченную структуру. Они занимают фиксированное положение и взаимодействуют друг с другом сильными силами притяжения. Это объясняет прочность и устойчивость твердых тел.
Однако, в любом веществе молекулы могут дезинтегрироваться на атомы в процессе химических реакций. Такие реакции могут приводить к изменению свойств вещества, образованию новых соединений и освобождению энергии. Молекулярная структура является основой для понимания и изучения таких реакций.
Таким образом, молекулярная структура определяет поведение вещества и его способность к дезинтеграции. Изучение этой структуры позволяет лучше понять свойства вещества и применить их в различных областях науки и техники.
Различные физические состояния
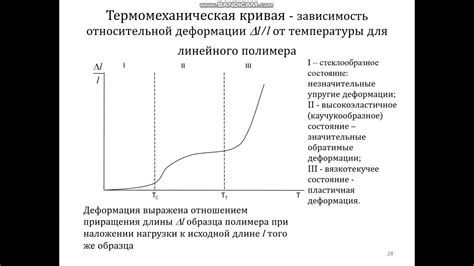
Материя может находиться в различных физических состояниях, таких как газообразное, жидкое и твердое. Каждое из этих состояний обладает своими уникальными свойствами и связано с различной степенью организации молекул.
В газообразном состоянии молекулы находятся в свободном движении и не связаны друг с другом. Они имеют высокую энергию и занимают большой объем. Из-за отсутствия сил притяжения между молекулами газообразные вещества могут дезинтегрироваться на молекулы и заполнять все имеющееся пространство.
В отличие от газов жидкости обладают большей степенью организации. Молекулы жидких веществ слабо связаны друг с другом и находятся в постоянном движении, но они более плотно упакованы. Это позволяет жидкостям обладать определенным объемом и формой. Однако, благодаря слабой связи между молекулами жидкости также могут дезинтегрироваться, но в меньшей степени, чем газы.
Твердые тела являются наиболее организованным состоянием материи. В них молекулы плотно упакованы и находятся в стабильном положении. Силы притяжения между молекулами в твердых телах очень сильны, что делает их структуру устойчивой и неизменной. Поэтому твердые тела не дезинтегрируются на молекулы.
Таким образом, различные физические состояния представляют собой градации организации молекул и связанных с этим свойств материи. Газы, жидкости и твердые тела отличаются по степени организации молекул, что определяет их способность к дезинтеграции и свойства в целом.
Связи между молекулами
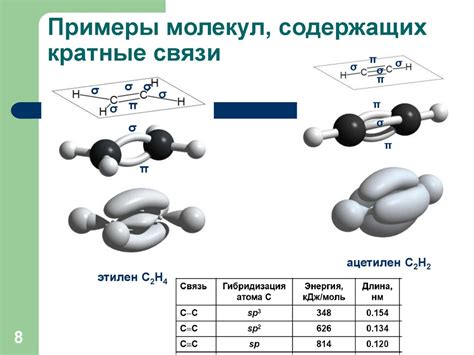
В жидкостях и твердых телах молекулы могут быть связаны различными типами взаимодействий. Одним из самых распространенных типов связей является ковалентная связь, при которой молекулы делят электроны и образуют ковалентные связи. Эти связи обеспечивают стабильность и прочность структуры вещества.
Другим важным типом связей между молекулами являются ван-дер-ваальсовы взаимодействия. Ван-дер-ваальсовы силы действуют между неполярными молекулами и обуславливают их сцепление. Эти силы слабые и могут быть легко преодолены при воздействии на вещество.
В некоторых случаях молекулы могут быть связаны также и водородными связями. Водородная связь состоит из электростатического притяжения между атомами водорода в одной молекуле и электронной оболочкой атомов кислорода, азота или фтора в другой молекуле. Водородные связи характеризуются высокой прочностью и часто наблюдаются в жидких и твердых телах.
Следует отметить, что связи между молекулами не являются абсолютно непроницаемыми. Возникающие воздействия, такие как тепловое движение, могут нарушить связь между молекулами и привести к дезинтеграции вещества. Однако, благодаря силам притяжения между молекулами, жидкости и твердые тела обладают достаточной стабильностью для сохранения своей структуры.
Устойчивость жидкостей и твердых тел
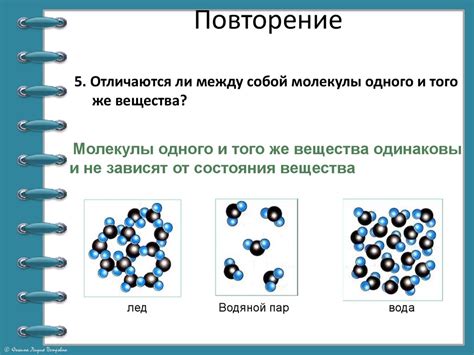
Жидкости и твердые тела обладают свойством устойчивости, благодаря которому они не дезинтегрируются на молекулы.
Причина этой устойчивости кроется в силе притяжения между молекулами вещества. В жидкостях и твердых телах молекулы находятся в близком расстоянии друг от друга и взаимодействуют силами притяжения, которые называются межмолекулярными силами.
Межмолекулярные силы поддерживают структуру и форму жидкостей и твердых тел. В жидкостях межмолекулярные силы слабее, что позволяет им принимать форму сосуда, в котором они находятся, и легко течь. Твердые тела же имеют сильные межмолекулярные силы, что придает им определенную форму, жесткость и устойчивость.
Межмолекулярные силы могут быть различного типа. В жидкостях преобладают силы ван-дер-Ваальса, которые обусловлены временными изменениями электрических зарядов в молекулах. В твердых телах также действуют силы ван-дер-Ваальса, а также ионо-дипольные и дипольные силы, возникающие между ионами и полярными молекулами.
Благодаря устойчивости жидкости и твердого тела, они могут сохранять свои свойства на протяжении длительного времени. Температура и давление могут повлиять на межмолекулярные силы и свойства вещества, что может привести к изменению его физических состояний или химических реакций.
Устойчивость жидкостей и твердых тел является фундаментальным свойством веществ, позволяющим им сохранять свою структуру и форму в условиях окружающей среды.
Энергетические барьеры

Энергетический барьер представляет собой потенциальную энергию, которую молекуле вещества необходимо преодолеть, чтобы изменить свое состояние или разорваться на отдельные молекулы. Этот барьер существует в твердых телах и жидкостях из-за сил взаимодействия между атомами или молекулами.
В твердых телах энергетический барьер высок, поэтому атомы или молекулы практически не могут изменять свое положение или оторваться от структуры. Это обусловлено сильными привлекательными силами между атомами, такими как ионные, ковалентные или металлические связи. Поэтому твердые тела обладают определенной формой и объемом, сохраняя свою структуру и свойства.
В жидкостях энергетический барьер ниже, и атомы или молекулы имеют возможность перемещаться и менять свое положение. В то же время, температура окружающей среды влияет на движение молекул, придавая им достаточную энергию для преодоления энергетических барьеров. Это объясняет способность жидкостей к течению и изменению их формы, однако они все равно обладают определенным объемом и ограниченной вязкостью.
Таким образом, наличие энергетического барьера обеспечивает стабильность и целостность твердых тел и жидкостей, предотвращая их дезинтеграцию на молекулы. Этот факт играет важную роль в прочности материалов и сохранении их физических свойств.
Термодинамические условия

Для понимания того, почему жидкости и твердые тела не дезинтегрируются на молекулы, необходимо обратиться к термодинамическим условиям, которые определяют поведение вещества и его состояние.
Вещество находится в определенном состоянии благодаря равновесию между двумя противоположными процессами - образованию и разрушению молекулярных связей. В любой системе существуют силы, которые стремятся разорвать эти связи, а также силы, которые их удерживают. Тепловое движение молекул вещества играет важную роль в поддержании равновесия.
Термодинамические условия для образования и дезинтеграции молекул определяются температурой и давлением. При достаточно высоких температурах или давлениях связи между молекулами могут разрушиться, что приведет к образованию газообразного состояния вещества.
Однако в типичных условиях, при которых мы обычно наблюдаем жидкости и твердые тела, эти связи остаются достаточно сильными, чтобы предотвратить дезинтеграцию на молекулы. Также следует отметить, что жидкости и твердые тела имеют более упорядоченную структуру, чем газы, благодаря чему они способны существовать в определенном состоянии.
Таким образом, термодинамические условия, такие как температура и давление, определяют способность вещества образовывать и сохранять свою структуру и предотвращать дезинтеграцию на молекулярный уровень.
Влияние внешних факторов

Одним из основных внешних факторов, влияющих на дезинтеграцию веществ, является температура. При повышении температуры, молекулы вещества получают больше энергии и начинают двигаться быстрее. Это может привести к нарушению молекулярной структуры и дезинтеграции вещества на молекулы или атомы.
Еще одним значительным фактором является давление. Под воздействием высокого давления, молекулы вещества могут быть сжаты и сближены друг с другом. Это может привести к увеличению сил притяжения между молекулами и их объединению в твердое тело.
Кроме того, вмешательство различных химических реакций может влиять на дезинтеграцию веществ. Химические реакции могут вызывать изменения в молекулярной структуре и связях между молекулами. В некоторых случаях, реакции могут привести к образованию новых соединений или обратным процессам дезинтеграции.
| Фактор | Влияние |
|---|---|
| Температура | Может приводить к дезинтеграции или объединению молекул вещества. |
| Давление | Высокое давление может привести к объединению молекул и образованию твердого тела. |
| Химические реакции | Могут вызвать изменение молекулярной структуры и связей молекул вещества. |
Результаты экспериментов и наблюдений

Множество экспериментов и наблюдений были проведены для понимания того, почему жидкости и твердые тела не дезинтегрируются на молекулы и сохраняют свою структуру и целостность.
Одним из ключевых факторов, определяющих устойчивость жидкостей и твердых тел, является межмолекулярное взаимодействие. Эксперименты показали, что внутри жидкости или твердого тела молекулы существуют вблизи друг друга и взаимодействуют между собой с помощью различных сил.
Такие силы, как ван-дер-Ваальсовы силы, электростатические силы и ковалентные связи, сохраняют молекулы в определенном порядке и предотвращают их разрушение. Уведомление об этом приводит к устойчивости структуры жидкости или твердого тела.
Эксперименты показали, что изменение условий окружающей среды, таких как температура и давление, может повлиять на интенсивность взаимодействий между молекулами. Например, при повышении температуры молекулы начинают двигаться быстрее, что может привести к изменениям во взаимодействии и, в конечном счете, к изменению состояния вещества.
Кроме того, существуют некоторые вещества, которые могут вызывать дезинтеграцию жидкостей и твердых тел. Это может происходить в результате химических реакций, при которых происходит разрыв связей между молекулами и образование новых соединений. Однако большинство веществ обладают структурой и химическими свойствами, которые обеспечивают их устойчивость и сохранение целостности.