Молекулы – это основные строительные блоки вещества, состоящие из атомов, связанных вместе. Но что происходит, когда молекулы разлетаются? Эта загадка давно привлекает внимание ученых и исследователей, и их поиски причин и механизмов этого явления продолжаются.
Первые попытки объяснить разлет молекул связывались с теорией хаоса и случайности. Согласно этой теории, молекулы разлетаются в результате столкновений и взаимодействий с другими частицами в системе. Однако, это объяснение не учитывает принципы сохранения энергии и момента импульса, а также не учитывает обратимость процесса.
Современные исследования подсказывают, что причины и механизмы разлетающихся молекул могут быть связаны с различными факторами. К таким факторам относятся температура, давление, концентрация и структура вещества. Изучение этих факторов и взаимодействий молекул является сложной задачей, требующей использования современных методов исследования, таких как компьютерное моделирование и экспериментальные данные.
Первичные факторы образования разлетающихся молекул
- Температура. Высокая температура способствует увеличению энергии молекул, что позволяет им разделиться и образовать разлетающиеся структуры.
- Давление. Повышенное давление также способствует разделению молекул и их переходу в разлетающее состояние.
- Концентрация. Высокая концентрация молекул облегчает их столкновения и взаимодействия, что может привести к образованию разлетающихся молекул.
- Химические реакции. Химические реакции могут вызывать изменения в структуре и энергии молекул, приводя к образованию разлетающихся молекул.
- Физические воздействия. Различные физические факторы, такие как воздействие света или электромагнитных полей, могут способствовать образованию разлетающихся молекул.
Первичные факторы образования разлетающихся молекул могут взаимодействовать друг с другом, создавая сложные процессы и механизмы. Понимание этих факторов и механизмов является важным для изучения разлетающихся молекул и их роли в различных процессах, таких как химические реакции, физические процессы и биологические системы.
Внешние источники энергии
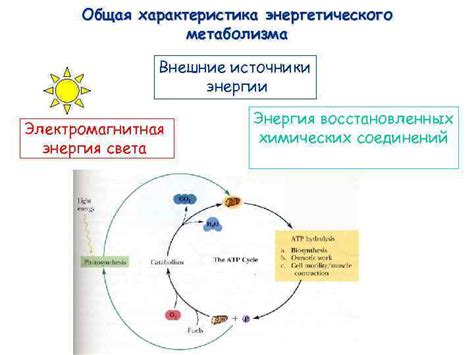
Для понимания механизмов разлетающихся молекул необходимо обратить внимание на роль внешних источников энергии. В процессе разлетания молекулы получают энергию, которая позволяет им преодолеть силы притяжения и двигаться в пространстве.
Одним из основных внешних источников энергии является тепловое излучение. Когда молекулы получают тепловую энергию, их скорость и кинетическая энергия увеличиваются, что приводит к разлетанию. Также, энергию могут поставлять другие виды излучения, такие как электромагнитные волны высокой частоты.
Другим важным источником энергии является механическая сила. Если на молекулу действуют силы, например, при столкновении с другой молекулой или поверхностью, то энергия передается от одной молекулы к другой и способствует их разлету.
Химические реакции также могут быть источником энергии для разлетающихся молекул. При химическом взаимодействии молекулы могут получать энергию от реакций, что способствует их разлету.
Таким образом, внешние источники энергии играют ключевую роль в процессе разлетающихся молекул. Они обеспечивают необходимую энергию, которая позволяет молекулам преодолевать силы притяжения и двигаться в пространстве.
Функции ферментов
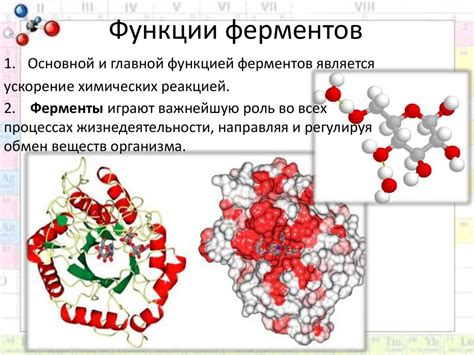
Ферменты имеют специфическую структуру и активный центр, который взаимодействует с молекулами субстрата и ускоряет реакцию. Некоторые ферменты, такие как амилаза и протеаза, помогают расщеплять молекулы на более простые компоненты, облегчая пищеварение.
Другие ферменты, такие как ДНК-полимераза и РНК-полимераза, играют важную роль в синтезе ДНК и РНК во время процесса репликации и транскрипции генетической информации. Ферменты также играют роль в процессе фотосинтеза, разрушая и синтезируя молекулы, необходимые для превращения света в энергию.
Они также участвуют в иммунной системе путем разрушения бактерий и вирусов. Некоторые ферменты используются в медицине и промышленности для производства лекарств и химических соединений.
Важной особенностью ферментов является их специфичность. Каждый фермент способен катализировать только определенную реакцию, так как его структура и активный центр подходят только для определенных субстратов.
Функции ферментов многообразны и важны для жизни организмов. Они обеспечивают ускорение и регулирование химических реакций, необходимых для поддержания жизнедеятельности клеток и организмов в целом.
Процессы, положительно влияющие на образование разлетающихся молекул
Термическая энергия: Одной из основных причин образования разлетающихся молекул является высокая температура. Тепловая энергия достаточно высокой степени помогает молекулам совершить быстрые и хаотичные движения, что приводит к их разъединению и образованию разлетающихся молекул.
Химические реакции: Некоторые химические реакции, особенно те, которые сопровождаются выделением большого количества энергии, могут привести к образованию разлетающихся молекул. Это происходит в результате скоростных химических процессов, которые вызывают разрушение молекулярных связей и образование новых соединений, высвобождающих кинетическую энергию.
Фотохимические реакции: При световых реакциях, когда молекулы взаимодействуют с фотонами света, возникает ионизация и разрыв химических связей. Это может привести к образованию разлетающихся молекул с большой энергией, так как световые реакции включают в себя высокоэнергетические стадии и реакции.
Ослабление межмолекулярных сил: Если межмолекулярные силы вещества ослаблены, например, при нагревании или воздействии других факторов, то это может способствовать образованию разлетающихся молекул. В отсутствие достаточной связующей силы, молекулы легко разлетаются и образуют разлетающиеся молекулы в газообразной форме.
Окислительно-восстановительные реакции
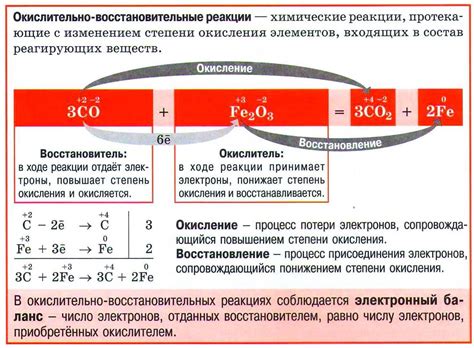
В окислительно-восстановительных реакциях происходит изменение степени окисления атомов. Атом, снимающий электроны, окисляется и превращается в положительный ион, а атом, передающий электроны, восстанавливается и превращается в отрицательный ион.
ОВ реакции играют важную роль во многих процессах, происходящих в живых организмах и в неорганической природе. Например, дыхание, фотосинтез, электролиз и многие другие процессы являются окислительно-восстановительными реакциями.
Передача электронов в ОВР может происходить как непосредственно между двумя атомами, так и через электрон-переносчики. Типичными электрон-переносчиками являются ионы и молекулы, способные существовать и в ионной, и в нейтральной форме, такие как кислород, водород, нитраты, ферроцианиды и др.
Окислительно-восстановительные реакции играют важную роль в промышленности, в особенности в производстве химических веществ, металлов и электрохимических элементов.
Примеры окислительно-восстановительных реакций включают в себя окисление железа, горение угля, фотосинтез, взаимодействие металлов с кислородом, реакции горения, реакции взаимодействия кислот и щелочей, электролиз воды и многие другие.
Тепловые изменения
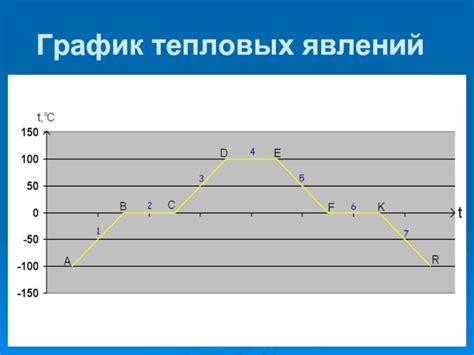
Тепловые изменения играют важную роль в процессе разлетающихся молекул. Под воздействием тепла, молекулы начинают двигаться более активно, что приводит к их разлетанию.
Тепло - это энергия, передаваемая от одного объекта к другому вследствие разности температур. В контексте разлетающихся молекул, тепло может быть представлено в виде движения тепловых частиц, таких как фононы, которые переносят тепловую энергию.
Под воздействием тепловой энергии, молекулы получают кинетическую энергию, что приводит к увеличению их скорости и движению в разные стороны. Более активные движения молекул способствуют их разлетанию в пространстве.
Тепловые изменения также могут вызвать изменения во внутренней структуре молекул, такие как изменение расстояния между атомами или изменение углов связей. Эти изменения внутри молекул также могут способствовать их разлетанию.
Важно отметить, что тепловые изменения могут быть вызваны различными факторами, такими как нагревание, воздействие света или химические реакции. Разные факторы могут вызвать различные тепловые изменения, что, в свою очередь, может повлиять на процесс разлетающихся молекул.
Механизмы разделения молекул на составные части

При термическом разложении молекулы подвергаются различным химическим реакциям, в результате которых образуются новые вещества. Эти реакции сопровождаются выделением энергии и увеличением количества свободных радикалов. Термическое разложение может происходить как спонтанно, так и под воздействием внешних факторов, таких как нагревание.
Еще одним механизмом разделения молекул является фотолиз - процесс разложения молекул под воздействием света. Фотолиз осуществляется за счет поглощения фотонов, что приводит к возбуждению электронов и изменению химических связей в молекулах. При этом молекулы могут разлагаться на ионы, атомы или более простые молекулы.
Кроме того, существует механизм разделения молекул под воздействием электрического тока. Этот процесс называется электролизом и основан на использовании электролитических ячеек. При электролизе молекулы разлагаются на ионы под влиянием электрического поля, которое создается при подведении тока к электродам. Разделенные ионы перемещаются к противоположным полярностям электродов и могут вступать в новые химические реакции.
Таким образом, механизмы разделения молекул на составные части включают в себя термическое разложение, фотолиз и электролиз. Каждый из этих механизмов имеет свои особенности и применяется в различных областях науки и промышленности.
Химические реакции

Химические реакции можно классифицировать по нескольким признакам. Одним из них является характер изменения вещества: окислительно-восстановительные реакции, кислотно-щелочные реакции, реакции образования осадков и т.д.
Окислительно-восстановительные реакции происходят при передаче электронов между веществами. В результате одно вещество окисляется (потеряет электроны), а другое вещество восстанавливается (получит электроны). Эти реакции являются основой процессов сгорания, окисления металлов и других важных химических превращений.
Кислотно-щелочные реакции происходят при взаимодействии кислот и щелочей, при которых образуется соль и вода. Кислоты выбрасывают водородные ионы H+, а щелочи выбрасывают гидроксидные ионы OH-. Эти ионы реагируют между собой, образуя воду и соль.
Реакции образования осадков происходят при смешении двух растворов, в которых содержатся соединения, образующие нерастворимые соли. В результате такой реакции образуются твердые частицы, осадок, который выпадает из раствора.
Химические реакции особо важны в жизни человека. Благодаря этим реакциям происходят такие процессы, как дыхание, пищеварение, синтез жизненно важных веществ в организмах, производство энергии и многое другое.
Физические процессы

Сила взаимодействия между молекулами также влияет на их разлет. В зависимости от рода взаимодействия, молекулы могут образовывать агрегаты или разлетаться во все стороны. Например, при сильном притяжении молекулы будут образовывать жидкость или твердое вещество, в то время как при слабом взаимодействии вещество будет газообразным.
Еще одним физическим процессом, влияющим на разлет молекул, является диффузия. Диффузия – это процесс перемещения молекул из области более высокой концентрации в область более низкой концентрации. Этот процесс осуществляется под воздействием теплового движения молекул и происходит до тех пор, пока концентрации не выровняются.
Кроме того, физические процессы могут влиять на разлет молекул через изменение давления и температуры. При изменении давления молекулы могут сдвигаться в ту или иную сторону, в зависимости от различия давлений. Также, увеличение температуры может увеличить кинетическую энергию молекул, что в свою очередь ускорит их движение и разлет.