Калий - это химический элемент, обладающий атомным номером 19 в периодической таблице. В природе существуют три стабильных изотопа калия: калий-39, калий-40 и калий-41. Причиной существования изотопов калия является его атомная структура и процессы ядерного распада.
Кальция атомный ядро состоит из протонов и нейтронов. Калий-39 (K-39) имеет 19 протонов и 20 нейтронов, калий-40 (K-40) имеет 19 протонов и 21 нейтрон, а калий-41 (K-41) имеет 19 протонов и 22 нейтрона. Количество протонов в атомном ядре определяет химические свойства элемента, а количество нейтронов влияет на его стабильность.
Существуют два основных процесса, которые приводят к образованию изотопов калия: альфа-распад и бета-распад. В альфа-распаде, ядро излучает альфа-частицу, состоящую из двух протонов и двух нейтронов. В результате этого процесса происходит изменение состава ядра и образование нового элемента с меньшим атомным номером.
Причины существования изотопов калия
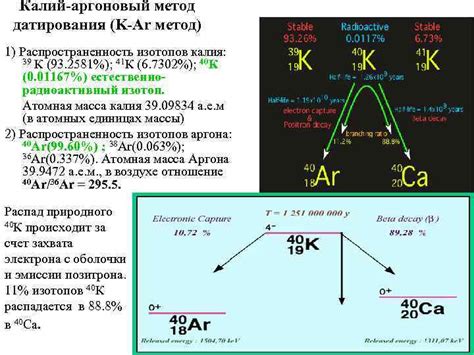
Главной причиной существования изотопов калия является ядерная структура этого элемента. Атомы элементов состоят из протонов, нейтронов и электронов. Количество протонов в ядре определяет химические свойства элемента, а количество нейтронов может варьироваться, создавая различные изотопы.
Неустойчивый изотоп калия-40 является особенно интересным, потому что он имеет способность претерпевать радиоактивный распад. При распаде калия-40 образуется аргон-40, и этот процесс называется калиевым методом датирования. Этот метод широко используется для определения возраста геологических образцов и археологических находок.
Существование различных изотопов калия также обусловлено процессами нуклеосинтеза, которые происходят в звездах. В результате ядерных реакций в звездных толчках и взрывах суперновых, образуются различные элементы, включая калий и его изотопы.
Изотопы калия также могут быть использованы в научных исследованиях и технологиях. Например, калий-39 используется в ядерной магнитной резонансной (ЯМР) спектроскопии, которая позволяет исследовать структуру, свойства и взаимодействие молекул.
Таким образом, причины существования изотопов калия связаны с физическими свойствами элемента, процессами нуклеосинтеза в звездах и научными исследованиями. Различные изотопы калия предоставляют нам возможность лучше понять природу и многообразие нашего мира.
Калий - элемент периодической системы
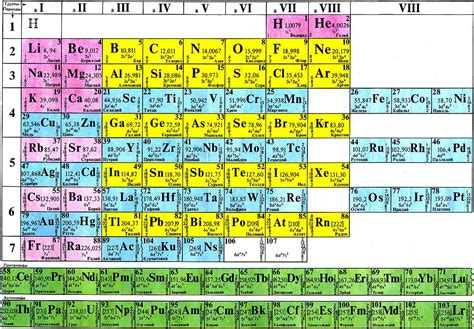
Калий относится к щелочным металлам и является сильным окислителем. В природе обычно встречается в виде солей, особенно хлорида калия (KCl) и сульфата калия (K2SO4).
Одной из уникальных характеристик калия является его способность образовывать изотопы. Изотопы - это атомы одного и того же элемента, но с разным числом нейтронов в ядре. В случае калия, существует три стабильных изотопа: калий-39, калий-40 и калий-41. Калий-39 является наиболее распространенным и составляет около 93% всех атомов калия на Земле.
Причины существования изотопов калия связаны с его строением ядра и стабильности различных комбинаций нейтронов и протонов. Калий-40 является радиоактивным изотопом и используется для определения возраста геологических образцов по методу калий-аргоновой датировки.
Изотопы калия имеют важное значение не только в геологии, но и в медицине и промышленности. Их свойства могут быть использованы для создания радиоактивных препаратов, в процессе облучения для лечения раковых заболеваний и в других сферах науки и техники.
Таким образом, причины существования изотопов калия связаны с его химическим строением и использованием его свойств в различных областях науки и техники.
Свойства изотопов калия

Самым распространенным изотопом калия является калий-39 (39K), который составляет около 93% всех атомов калия на Земле. Его ядро состоит из 19 протонов и 20 нейтронов. Изотоп калия-39 является стабильным и не радиоактивным.
Однако, среди изотопов калия также присутствуют радиоактивные формы. Изотоп калия-40 (40K) имеет 19 протонов и 21 нейтрон в ядре. Он является единственным радиоактивным изотопом калия и обладает полувеком распада около 1,25 миллиарда лет. Это делает его полезным инструментом для определения возраста геологических и археологических образцов методом радиоизотопного датирования.
Изотоп калия-41 (41K) также присутствует в природе, но его содержание очень низкое - около 0,012%. Образец калия с высоким содержанием изотопа калия-41 может быть использован в методах спектроскопии для измерения электронных, магнитных и других свойств вещества.
- Калий-39 (39K) - стабильный изотоп в основе состава калия на Земле.
- Калий-40 (40K) - радиоактивный изотоп, используемый в методе радиоизотопного датирования.
- Калий-41 (41K) - редкий изотоп, используемый в спектроскопии для измерения свойств вещества.
Изотопы калия имеют различные свойства и делятся на стабильные и радиоактивные формы. Эти изотопы играют важную роль в различных научных исследованиях, а также в промышленности и медицине.
Процессы образования изотопов калия

Существует несколько причин, объясняющих образование изотопов калия.
Во-первых, существуют естественные ядерные реакции, в результате которых в атоме калия могут происходить изменения числа нейтронов. Это может произойти вследствие захвата или выброса нейтрона атомом калия.
Во-вторых, один из изотопов калия, ^40K, образуется в результате радиоактивного распада других элементов. В частности, ^40K образуется при распаде ^40Ca. Этот изотоп имеет долгий период полураспада, поэтому он может существовать в природе в значительном количестве.
И, наконец, существуют и другие процессы образования изотопов калия, такие как ядерные реакции с участием других элементов или искусственное создание изотопов в научных лабораториях.
Распространение изотопов калия в природе
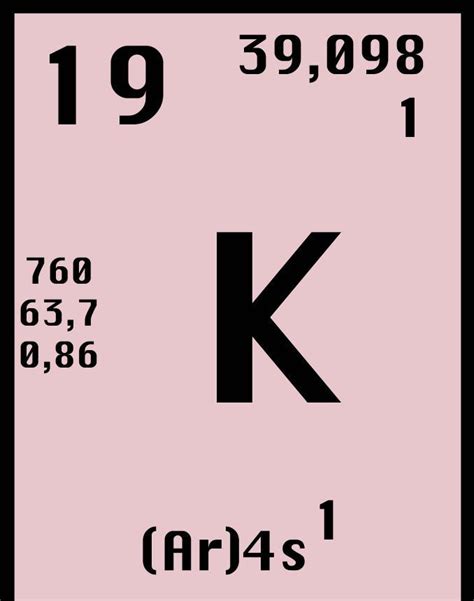
Интересно отметить, что радиоактивный изотоп калия-40 имеет долгий период полураспада (около 1,28 миллиарда лет), что позволяет его использование в ряде геологических и археологических исследований. Именно благодаря наличию калия-40 ученые смогли установить возраст Земли и определить времена геологических эпох.
Распространение изотопов калия в природе может варьироваться в зависимости от географического положения. Например, в морской воде концентрация изотопа калия-40 может быть ниже, чем в пресной воде или почве. Также известно, что растения и животные имеют немного различный состав изотопов калия, в зависимости от их места обитания и пищевых привычек.
Изотопы калия играют важную роль в жизни организмов. Например, калий-40 является основным источником радиоактивности в человеческом теле и используется для рентгеновских и радиоизотопных исследований.
Итак, распространение изотопов калия в природе является интересной исследовательской темой, позволяющей лучше понять процессы, происходящие на Земле и в живых организмах.
Практическое применение изотопов калия
Изотопы калия нашли свое применение в различных областях науки и промышленности.
Одним из основных практических применений является использование изотопа калия-39 в исследованиях по геологии и геохимии. Калий-39 является стабильным изотопом и используется для определения возраста горных пород методом кали-аргоновой датировки.
Изотоп калия-40, в свою очередь, применяется в радиоактивных методах датировки, таких как метод аргон-аргоновой датировки и рубидий-стронциевой датировки. Эти методы позволяют определить возраст различных геологических объектов, включая вулканические породы и минералы. Благодаря этому, изотоп калия-40 является важным инструментом для изучения истории Земли.
Другое практическое применение калия-40 заключается в его использовании для производства радионуклидов для медицинских исследований и терапии. Кристаллы бромида калия-40 можно облучать нейтронами, чтобы получить радиоактивные изотопы, которые могут использоваться для лечения рака и для маркировки молекул в медицинских исследованиях.