Соединение атомов является основным процессом, позволяющим образование всех веществ в нашей Вселенной. При этом, однако, совершается впечатляющий физический феномен - выделение энергии. Этот процесс, известный как экзотермическая реакция, обеспечивает не только эволюцию и превращение элементов, но и жизненно важные процессы на Земле, такие как горение и обогрев. Научное объяснение этого феномена состоит из нескольких ключевых факторов.
Первый фактор, ответственный за выделение энергии при соединении атомов, - это изменение электронных оболочек атомов в реакционном превращении. Когда два или более атома соединяются, их электронные оболочки переходят в более стабильное состояние. Такой переход сопровождается выделением энергии, так как стабильные электронные оболочки атомов находятся в состоянии более низкой энергии, чем нестабильные оболочки исходных атомов.
Второй фактор, влияющий на выделение энергии при соединении атомов, - это образование и разрушение химических связей. Соединение атомов обычно сопровождается образованием новых химических связей и разрушением старых. Образование более сильных химических связей вещества приводит к освобождению энергии, так как эти связи обладают меньшей энергией, чем исходные слабые связи.
Важно отметить, что выделение энергии при соединении атомов связано с законами сохранения энергии и массы. При образовании новых веществ с помощью соединения атомов, высвобождаемая энергия компенсирует энергетические потери, которые могут произойти в результате разрушения старых связей. Однако, это выделение энергии может воздействовать на природу реакции, делая ее экзотермической или эндотермической.
Причины выделения энергии

Эндоэнергетический процесс – это процесс, при котором система поглощает энергию из внешней среды. При соединении атомов с образованием химической связи, эндоэнергетический процесс характеризуется поглощением энергии. Это происходит потому, что энергия необходима для преодоления электростатического отталкивания зарядов атомов и растяжения связи до оптимальной длины.
Экзоэнергетический процесс – это процесс, при котором система выделяет энергию в окружающую среду. Подобный процесс происходит при образовании химической связи между атомами. При образовании связи система переходит к более устойчивому энергетическому состоянию, что означает ниже энергетическое положение. Избыточная энергия освобождается в форме тепла или света.
| Процесс | Энергия | Пример |
|---|---|---|
| Эндоэнергетический | Поглощение | Фотохимические реакции |
| Экзоэнергетический | Выделение | Сжигание топлива |
Причины выделения энергии при соединении атомов определяются характером взаимодействия зарядов и изменением энергии связи в результате образования новой связи. Это процесс, важный для понимания реакций, происходящих в природе и позволяющий объяснить явления, такие как горение, фотосинтез и синтез химических веществ.
При соединении атомов:
1. Освобождается энергия благодаря образованию более стабильных химических связей. При соединении атомы устраиваются в таком порядке, чтобы максимально уменьшить энергию, что приводит к выпуску энергии.
2. Образуется энергия связи. При соединении атомы образуют новые, более прочные связи, что приводит к выделению энергии.
3. Происходит экзотермическая реакция. При соединении атомов происходит экзотермическая реакция, при которой выделяется энергия в виде тепла или света.
4. Происходит уменьшение потенциальной энергии системы. При соединении атомов происходит снижение потенциальной энергии системы, что приводит к выделению энергии.
- 5. Освобождается энергия при переходе электронов. При соединении атомов происходит передача электронов между атомами, при которой выделяется энергия.
- 6. Образуется энергетически выгодный продукт. При соединении атомов образуется новое вещество с более низкой энергией, что приводит к выделению энергии.
Химические реакции

Химическая реакция представляет собой процесс, при котором происходит изменение взаимного расположения атомов, ионофов или молекул, что приводит к образованию новых веществ с изменёнными свойствами. Химические реакции можно классифицировать по различным признакам:
- По типу веществ, участвующих в реакции: реакции с участием элементов, реакции с участием соединений, реакции с участием смесей.
- По направлению протекания: прямые и обратимые реакции.
- По кинетической скорости: быстрые и медленные реакции.
- По фазовому состоянию веществ: газовые, жидкостные и твердотельные реакции.
Химические реакции являются основой для объяснения явлений, происходящих в живой и неживой природе. Они играют важную роль в химии, биологии, физике и многих других научных дисциплинах.
Одной из важных характеристик химических реакций является энергия, которая выделяется или поглощается в процессе реакции. В зависимости от того, является ли реакция эндотермической (поглощение энергии) или экзотермической (выделение энергии), происходит изменение энергии связи атомов в исходных и конечных веществах.
Изменение связей и электронного строения
В процессе химической реакции происходит перераспределение электронов между атомами. Атомы стремятся достичь наименьшей энергетической конфигурации, в которой их внешние энергетические уровни будут полностью заполнены или окажутся полностью пустыми. Для этого атомы могут обменивать электроны друг с другом.
В химической реакции ковалентной связью атомы делят между собой пару электронов. При этом образуется молекула, в которой атомы становятся связанными, что позволяет им достичь более устойчивого электронного строения. Образование ковалентной связи сопровождается выделением энергии и освобождением тепла, которые могут использоваться для световых, тепловых или химических процессов.
Другая форма связи - ионная связь, возникающая между атомами с разными зарядами. В процессе ионизации один атом отдает электрон(ы), а другой атом принимает его. Таким образом, образуется пара ионов с противоположными зарядами, которая обладает большей стабильностью и нижней энергией. Роспускание ионной связи требует энергии, в то время как ее образование выделяет энергию.
Изменение связей и электронного строения в химических реакциях играет важную роль во многих аспектах нашей жизни, от процессов пищеварения до производства энергии. Понимание этих процессов позволяет развивать новые материалы, улучшать технологии и создавать более эффективные способы использования энергии.
Образование более стабильных соединений

При реакциях образования химических соединений происходит объединение атомов в связи. Взаимодействие атомов позволяет им достигнуть более низкой энергетической конфигурации, что в свою очередь способствует образованию стабильных соединений.
| Соединение | Энергия связи (кДж/моль) |
|---|---|
| Водород (H2) | 432 |
| Кислород (O2) | 498 |
| Вода (H2O) | 458 |
| Углекислый газ (CO2) | 796 |
| Метан (CH4) | 524 |
В таблице представлены значения энергии связи для некоторых химических соединений. Они показывают, что при образовании стабильных молекул выделяется энергия.
Образование более стабильных соединений происходит за счет снижения потенциальной энергии системы и наличия более устойчивой структуры. Это связано с достижением оптимального расположения электронов во внешних оболочках атомов и образованием энергетически выгодных связей.
Таким образом, образование более стабильных соединений является важным фактором, вызывающим выделение энергии при соединении атомов и играющим решающую роль во многих химических реакциях.
Выделение энергии и избыток электронов
При соединении, например, атома металла и атома неметалла, происходит передача электронов от одного атома к другому. Избыток электронов на одном атоме и их дефицит на другом атоме создают электрическое поле, которое притягивает атомы друг к другу. Этот процесс называется ионной связью.
Подобные реакции сопровождаются освобождением энергии, так как образование ионной связи обеспечивает более устойчивое состояние системы. В результате этой реакции, энергия, необходимая для разрыва старых связей и создания новых связей, освобождается в виде тепла или света. Таким образом, выделение энергии при соединении атомов является следствием образования более стабильных химических связей между атомами.
Выделение энергии при соединении атомов играет важную роль во многих физических и химических процессах. Оно позволяет использовать энергию, выделяющуюся при реакциях, для различных нужд человека. Примером такого использования является генерация электроэнергии в химических аккумуляторах, где происходит управляемое освобождение энергии при реакциях соединения и разъединения атомов.
Образование химических связей
Основной механизм образования химической связи – общая валентность атомов. Атомы стремятся набрать определенное количество электронов во внешней оболочке, чтобы достигнуть наиболее стабильного энергетического состояния. Это можно достичь путем образования химических связей с другими атомами.
При образовании химической связи энергия отдельных атомов суммируется, что приводит к образованию более стабильной системы, а следовательно, к выделению энергии. Эта выделенная энергия может быть использована для выполнения работы или нагревания окружающей среды.
Образование химических связей играет ключевую роль в химических реакциях и процессах, определяющих свойства и поведение вещества. Понимание этого процесса позволяет контролировать химические реакции и создавать новые вещества с желаемыми свойствами.
Уменьшение потенциальной энергии системы
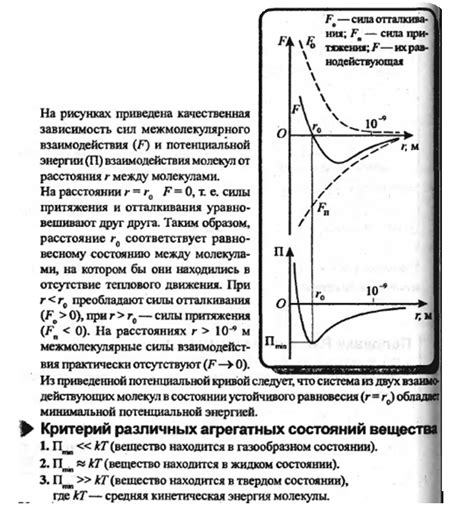
Потенциальная энергия системы определяется взаимодействиями частиц внутри нее. При соединении атомов происходит изменение расстояния между ними, а значит, изменяется потенциальная энергия системы. Если в результате соединения атомов потенциальная энергия уменьшается, то освобождающаяся энергия называется энергией образования связи.
Основной механизм уменьшения потенциальной энергии при соединении атомов заключается в образовании химической связи. Под влиянием электростатических сил и других факторов, атомы вступают во взаимодействие и формируют более стабильное состояние, чем в отдельности. Это приводит к уменьшению расстояния между атомами и, следовательно, к снижению потенциальной энергии системы.
| Первый атом | Второй атом | Потенциальная энергия |
|---|---|---|
| Атом 1 | Атом 2 | Высокая |
| Связанные атомы 1 | Связанные атомы 2 | Низкая |
Как видно из таблицы, потенциальная энергия системы уменьшилась после образования связи между атомами, что свидетельствует о выделении энергии при соединении атомов. Энергия образования связи может быть высвобождена в виде тепла или света, что является основой многих химических реакций и процессов.