Медь – один из самых известных и широко используемых металлов в мире. Его свойства делают его неотъемлемой частью нашей повседневной жизни. Однако, мало кто задумывается о том, почему, несмотря на свою активность, медь не реагирует с водой. В данной статье мы рассмотрим причины этого феномена и попытаемся объяснить его научно.
Медь – весьма активный металл, который может взаимодействовать с многими веществами. Он обладает высокой электрической и теплопроводностью и используется во множестве отраслей, включая электронику, строительство и медицину. Однако, когда дело доходит до взаимодействия с водой, медь оказывается неотзывчивой. Почему так происходит?
Ответ кроется в реакции меди с кислородом. Когда медь контактирует с кислородом в воздухе, происходит окисление металла, образуется слой окиси меди, который защищает металл от дальнейшей коррозии. Вода, в свою очередь, содержит молекулы кислорода, но в намного меньших концентрациях, чем воздух. Поэтому, когда медь погружается в воду, окисление не происходит в таких же масштабах, и медь не реагирует с водой так, как она реагирует с воздухом.
Причины отсутствия реакции меди с водой

Одной из главных причин отсутствия реакции меди с водой является ее защитная оксидная пленка. Воздействие кислорода из воздуха приводит к образованию тонкого слоя оксидов на поверхности меди. Эта оксидная пленка предотвращает дальнейшее окисление меди путем создания барьера между металлом и водой, не позволяя атомам кислорода и водорода входить в реакцию с медью.
Кроме того, медь, особенно в чистой форме, не обладает способностью к свободному и быстрому движению атомов вещества. Для химической реакции необходимо, чтобы молекулы воды разрушали образующиеся на поверхности меди оксиды и взаимодействовали с металлом. Ограниченная подвижность атомов меди препятствует этому процессу и делает реакцию невозможной.
Таким образом, причины отсутствия реакции меди с водой заключаются в низкой активности меди, наличии защитной оксидной пленки и ограниченной подвижности атомов металла. Эти факторы объясняют стабильность меди в условиях контакта с водой и отсутствие химической реакции между ними.
Физические свойства меди

Одной из основных характеристик меди является ее высокая электропроводность. Медь считается одним из самых хороших проводников электричества, что делает ее незаменимой в производстве проводов, кабелей и другой электроэнергетической аппаратуры. Кроме того, она обладает также высокой теплопроводностью, что позволяет использовать медь в производстве теплообменных систем.
Медь также обладает высокой пластичностью, благодаря чему легко поддается различным видам обработки, включая прокатку, волочение и формование. Это позволяет применять медь для создания различных изделий и компонентов, таких как трубы, проволока и листовой металл.
Однако медь имеет также некоторые недостатки. Например, она может быть склонна к образованию пятен и железных взаимодействиях, что может привести к ее коррозии. Кроме того, медь является мягким металлом, что делает ее менее устойчивой к механическим повреждениям и истиранию.
- Медь имеет химический символ Cu и высокую электропроводность.
- У меди также высокая теплопроводность и пластичность.
- Однако медь может быть склонна к коррозии и механическим повреждениям.
Влияние оксидации

Когда медь взаимодействует с воздухом и водой, на её поверхности начинается процесс окисления. В результате этого процесса образуется тонкая слой оксида меди, который немного растворим в воде и способен предотвратить дальнейшее взаимодействие меди с водой.
Образование оксидной пленки является важной защитной реакцией, которая защищает медь от дальнейшей коррозии и разрушения. Это объясняет, почему медные трубы, предназначенные для транспортировки воды, могут служить десятилетиями без каких-либо видимых признаков повреждения.
Кроме того, оксид меди обладает пористой структурой, которая позволяет ему проникать вглубь металла и создавать ещё более надёжную защитную пленку. Этот процесс называется пассивацией и является еще одной причиной, по которой медь не реагирует с водой.
Таким образом, оксидация меди и образование оксидной пленки являются ключевыми факторами, которые объясняют, почему медь не реагирует с водой и является одним из наиболее устойчивых металлов к коррозии и окислению.
Стабильность химической связи
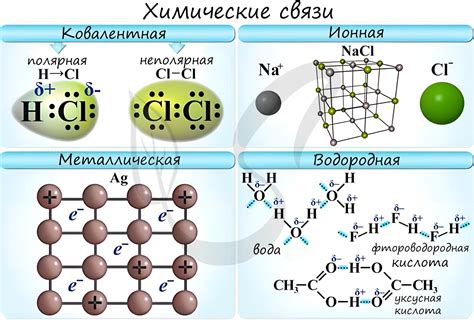
Почему медь не реагирует с водой? Причина кроется в стабильности химической связи, которая образуется между медью и ее окружением.
Медь является химическим элементом с относительно низкой реактивностью и стабильными химическими свойствами. Она образует стабильные и прочные связи с другими элементами, включая воду. Это связано с ее электронной структурой и расположением в периодической таблице.
Вода, в свою очередь, является молекулой, состоящей из атомов водорода и кислорода. Атомы водорода образуют ковалентную связь с атомом кислорода, образуя стабильную молекулу воды. Медь не имеет склонности образовывать ковалентные связи с атомами водорода, поэтому не реагирует с водой.
Кроме того, медь обладает высокой стойкостью к окислению. Ее поверхность покрывается тонким слоем оксида, который образуется в результате взаимодействия меди с кислородом воздуха. Этот слой оксида служит своеобразной защитной пленкой, препятствующей дальнейшему окислению меди и реакции с водой.
Таким образом, стабильность химической связи и высокая стойкость к окислению делают медь нереактивной с водой и позволяют ей служить важным строительным и электротехническим материалом.
Реакция с воздухом и окисление

Окисление меди происходит благодаря взаимодействию с кислородом из воздуха. Реакция меди с кислородом и образование оксида меди может быть представлена следующим уравнением:
- 2Cu + O2 → 2CuO
При окислении меди образуется оксид меди (II), который имеет керамическую структуру и обладает антибактериальными свойствами. Это объясняет широкое использование меди в медицинских изделиях и поверхностях.
Однако, в отличие от стальных материалов или железа, оксид меди образует защитную пленку на поверхности меди, которая предотвращает дальнейшее окисление металла. Эта патина является стабильной и предотвращает дальнейшую реакцию меди с кислородом из окружающего воздуха. Поэтому, независимо от продолжительности контакта меди с воздухом, она остается относительно устойчивой к дальнейшему окислению.
Тем не менее, при продолжительном воздействии воды на поверхность меди может быть заметно усиление процесса окисления. В этом случае, на поверхности меди может образоваться зеленоватая патина, состоящая из карбонатов и гидроксидов меди. Это объясняется наличием воды, которая усиливает взаимодействие с кислородом и другими возможными реагентами, содержащимися в атмосфере.