Таблица Менделеева является одним из главных инструментов в химии, позволяющим систематизировать и классифицировать элементы. Она позволяет нам легко ориентироваться в обширном мире химических элементов и их свойств. Одной из основных групп элементов в таблице Менделеева являются неметаллы, обладающие особым набором свойств.
Неметаллы - это элементы, обладающие способностью образовывать соединения с металлами и другими неметаллами. Они находятся справа от ступеней таблицы Менделеева и включают такие элементы, как кислород, азот, сера, фосфор и другие. Каждый из этих элементов обладает своими уникальными свойствами, которые определяют их поведение в химических реакциях и взаимодействиях с другими веществами.
В таблице Менделеева неметаллические свойства элементов возрастают по мере движения слева направо и сверху вниз в группах. Факторы, определяющие увеличение неметаллических свойств в таблице Менделеева, включают атомный радиус, электроотрицательность и энергию ионизации. Малый атомный радиус и высокая электроотрицательность увеличивают неметаллические свойства элементов, так как они способствуют более сильному притяжению электронов валентной оболочки и большей агрессивности в химических реакциях.
Раздел 1: Что влияет на увеличение неметаллических свойств?
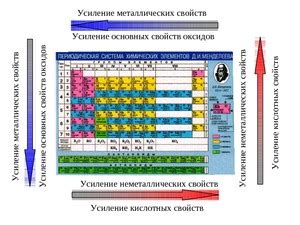
Также на увеличение неметаллических свойств влияет радиус атома. Неметаллы часто имеют маленький радиус, что обусловлено сильным притяжением ядра к внешним электронам. Благодаря этому, неметаллы могут образовывать сильные ковалентные связи и обладать высокой электроотрицательностью.
Другой фактор, влияющий на увеличение неметаллических свойств, - энергия ионизации. Энергия ионизации - это энергия, необходимая для удаления одного электрона из атома. Чем выше энергия ионизации, тем больше вероятность, что элемент будет обладать неметаллическими свойствами.
Важной закономерностью является также положение элемента в группе таблицы Менделеева. Неметаллические свойства в целом возрастают по мере приближения к верхнему правому углу группы. Это связано с увеличением электроотрицательности и энергии ионизации в этом направлении.
Таким образом, увеличение неметаллических свойств обусловлено электроотрицательностью, радиусом атома, энергией ионизации и положением элемента в таблице Менделеева. Эти факторы взаимосвязаны и определяют химические свойства элементов.
Раздел 2: Факторы увеличения неметаллических свойств в таблице Менделеева
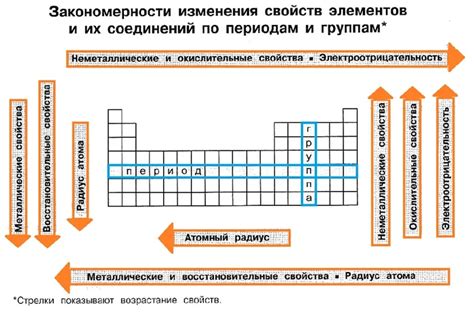
В таблице Менделеева представлены все известные химические элементы, в том числе и неметаллы. Неметаллы имеют свойства, отличающие их от металлов, включая низкую электропроводность, неяркую поверхность и способность образовывать простые соединения с металлами.
Факторы, влияющие на увеличение неметаллических свойств элементов в таблице Менделеева, можно выделить следующие:
- Электроотрицательность: неметаллы обладают более высокой электроотрицательностью, чем металлы. Чем выше значение электроотрицательности элемента, тем больше вероятность, что он будет обладать неметаллическими свойствами.
- Электронная конфигурация: неметаллы обычно имеют электронную конфигурацию, в которой валентная оболочка не полностью заполнена. Недостаток электронов в валентной оболочке позволяет неметаллам легко принимать или получать электроны, что способствует их реакционной активности.
- Радиус атома: неметаллы обычно имеют меньший радиус атома по сравнению с металлами. Малый радиус атома способствует сжатию электронной оболочки, что делает неметаллы более электронегативными.
- Ионизационная энергия: неметаллы обладают высокой ионизационной энергией, то есть энергией, необходимой для удаления электрона из атома. Высокие значения ионизационной энергии делают неметаллы менее склонными к образованию ионов положительного заряда и более склонными к образованию отрицательных ионов.
Таким образом, электроотрицательность, электронная конфигурация, радиус атома и ионизационная энергия являются факторами, приводящими к увеличению неметаллических свойств в таблице Менделеева.
Раздел 3: Закономерности в увеличении неметаллических свойств по периодам и группам
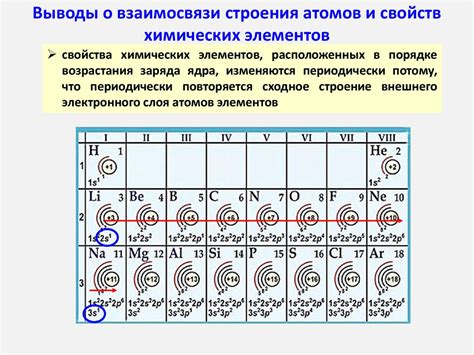
В таблице Менделеева можно наблюдать определенные закономерности в увеличении неметаллических свойств по периодам и группам. Периоды в таблице Менделеева указывают на количество электронных оболочек, которыми обладает элемент. Следовательно, с увеличением номера периода происходит увеличение энергии электронных оболочек, что в свою очередь влияет на химические свойства элементов.
В периоде, по мере увеличения номера, наблюдается увеличение электроотрицательности элементов. Электроотрицательность характеризует способность атома притягивать к себе электроны в химической связи. Более высокая электроотрицательность делает элемент более неметаллическим, так как он имеет большую тенденцию к привлечению электронов.
Сходная закономерность наблюдается и в группах таблицы Менделеева. Группы - это вертикальные столбцы элементов, которые имеют одинаковое количество электронов на внешней энергетической оболочке. В одной группе элементы имеют сходные химические свойства, в том числе и неметаллическую структуру.
Таким образом, общая закономерность заключается в том, что с увеличением номера периода или группы в таблице Менделеева происходит увеличение неметаллических свойств элементов. Это связано с изменением энергии электронных оболочек и увеличением электроотрицательности атомов.