Когда мы говорим об атомах их различных свойствах, одна из ключевых характеристик, на которую мы обращаем внимание, это количество нейтронов, содержащихся в атоме. Нейтроны играют важную роль в структуре и стабильности атома, и их количество может варьироваться в разных атомах одного элемента.
Но как узнать количество нейтронов в атоме? Для начала, необходимо знать атомный номер элемента, который можно найти в периодической таблице химических элементов. Атомный номер определяется количеством протонов в ядре атома. Он показывает, сколько электронов и протонов содержит атом.
Чтобы узнать количество нейтронов в атоме, нужно выполнить следующий простой расчет: вычесть атомный номер из общего числа нуклонов. Общее число нуклонов в атоме (протоны + нейтроны) можно найти, посмотрев на массовое число элемента в периодической таблице.
Например, если у нас есть атом кислорода (O), атомный номер которого равен 8, а его массовое число равно 16, то количество нейтронов можно вычислить по следующей формуле: 16 - 8 = 8. Таким образом, в атоме кислорода содержится 8 нейтронов.
Таким образом, зная атомный номер элемента и массовое число, можно легко определить количество нейтронов в атоме. Эта информация полезна для понимания структуры атома и его химических свойств.
Виды атомов и их структура

В каждом атоме количество протонов и электронов совпадает, что придает атому электрическую нейтральность. Протоны имеют положительный заряд, электроны - отрицательный, их заряды равны по величине.
Нейтроны, как следует из их названия, не имеют электрического заряда. Количество нейтронов в атоме может быть разным и определяет его изотоп. Изотопы - это разновидности одного и того же элемента, отличающиеся только количеством нейтронов в атоме.
Изотопы могут иметь различные физические и химические свойства, но у них сохраняются общие характеристики, связанные с их атомной структурой. Изучение различных видов атомов и их структуры является основой для понимания многих химических и физических явлений.
Заряд ионов и количество нейтронов
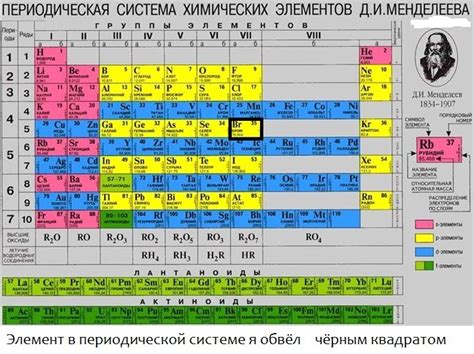
Количество нейтронов в атоме можно вычислить, зная его атомный номер и массовое число. Массовое число атома равно сумме протонов и нейтронов в ядре атома. Атомный номер же представляет собой количество протонов в атоме. Для определения количества нейтронов достаточно вычесть атомный номер из массового числа:
Количество нейтронов = массовое число - атомный номер
Кроме того, для атомов и ионов может быть характерным ионный заряд. Ионный заряд показывает, сколько электронов должно быть воспринято или отдано атому или иону, чтобы он стал электрически заряженным. Отличие иона от атома заключается в наличии положительного или отрицательного заряда. Если атом принял или отдал электрон, ему приписывается положительный или отрицательный заряд.
Заряд иона можно вычислить, зная количество протонов и электронов в атоме. Если количество протонов и электронов одинаково, то заряд атома нейтральный и равен нулю. В случае, если электронов больше, чем протонов, атом будет иметь отрицательный заряд. Если же протонов больше, чем электронов, заряд будет положительным. Разница в количестве протонов и электронов определяет величину заряда иона.
| Знак | Описание |
|---|---|
| + | Положительный заряд (катион) |
| - | Отрицательный заряд (анион) |
| 0 | Нейтральный заряд (атом) |
Таблица Менделеева и количество нейтронов
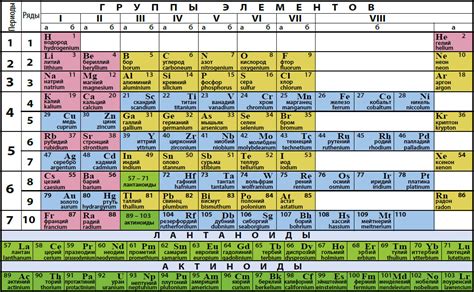
Одна из самых важных характеристик элемента, которую можно найти в таблице Менделеева, - это количество нейтронов в его атоме.
Количество нейтронов в атоме определяет массу элемента и его химические свойства. Нейтроны не имеют электрического заряда и находятся в ядре атома вместе с протонами.
В таблице Менделеева количество нейтронов может индицироваться различными способами. Один из распространенных способов - упоминание массового числа элемента. Массовое число - это сумма протонов и нейтронов в ядре атома.
Например, для элемента кислород (O) массовое число равно приблизительно 16. Таким образом, кислород имеет приблизительно 16 нейтронов в своем атоме.
Понимание количества нейтронов в атоме элемента позволяет ученым более глубоко изучать его свойства и взаимодействия с другими элементами.
| Элемент | Символ | Массовое число | Количество нейтронов |
|---|---|---|---|
| Кислород | O | 16 | 16 |
| Углерод | C | 12 | 12 |
| Железо | Fe | 56 | 30 |
| Алюминий | Al | 27 | 14 |
В таблице выше приведены некоторые примеры элементов и количество нейтронов в их атомах в соответствии с их массовыми числами.
Таблица Менделеева является не только важным инструментом для химиков, но и интересной и познавательной информацией для всех, интересующихся миром элементов и химии в целом.
Методы определения количества нейтронов

Для определения количества нейтронов в атоме существуют различные методы, которые основываются на принципах ядерной физики и различных техниках.
Один из распространенных методов - это метод масс-спектрометрии. Он основан на измерении отношения массы атома к его заряду. Путем анализа этих данных можно получить информацию о количестве нейтронов в атоме.
Другой метод - это метод измерения ядерных реакций. При проведении определенных ядерных реакций возможно измерение количества выделенных или потребленных нейтронов. Исходя из этих данных можно определить количество нейтронов в атоме.
Также существуют методы, которые основаны на использовании специальных изотопов. Изотопы имеют одинаковое количество протонов, но различное количество нейтронов. Анализируя показатели измерений с использованием таких изотопов, можно определить количество нейтронов в атоме.
Все эти методы имеют свои особенности, преимущества и ограничения. Их выбор зависит от конкретных условий и требований эксперимента. При измерении количества нейтронов необходимо учитывать множество факторов, таких как точность измерений, фоновые шумы и так далее.
Важно понимать, что определение количества нейтронов в атоме является сложным и не всегда точным процессом. Однако, благодаря современным технологиям и методам, ученые постоянно совершенствуют способы определения количества нейтронов, что позволяет получить все более точные результаты.
Использование нейтронных изотопов
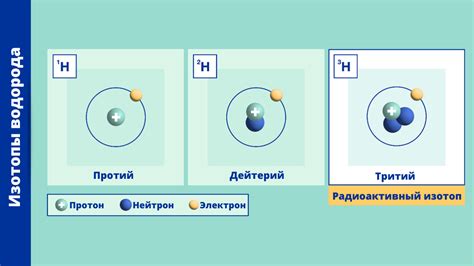
Одним из основных методов использования нейтронных изотопов является нейтронная активация. В этом процессе нейтроны взаимодействуют с ядрами атомов, превращая их в радиоактивные изотопы. Затем можно изучать полученные радиоактивные изотопы, чтобы получить информацию о составе и структуре образца.
В медицине нейтронные изотопы используются для диагностики и лечения различных заболеваний. Например, изотоп бора-10 используется в бороновой нейтронной захваточной терапии для лечения рака. Нейтроны взаимодействуют с изотопом бора-10, вызывая выброс альфа-частиц, которые разрушают опухоль.
Кроме того, нейтронные изотопы используются в промышленности для контроля качества материалов. Неоднородности и дефекты в структуре материала могут быть обнаружены с помощью нейтронных лучей, которые проходят через образец и регистрируются на детекторе.
Использование нейтронных изотопов помогает расширить наши знания о мире атомов и молекул, а также применить эту информацию в различных областях науки и технологии.
Техники экспериментального определения

Определение количества нейтронов в атоме может быть осуществлено с использованием различных экспериментальных методов. Рассмотрим некоторые из них:
| 1. Использование спектроскопии |
| Этот метод основан на измерении энергетических уровней атома. С помощью спектроскопии можно определить разницу в энергии между уровнями, связанную с наличием нейтронов. Путем сравнения экспериментальных данных с известными значениями энергетических уровней можно определить количество нейтронов в атоме. |
| 2. Использование ядерных реакций |
| Этот метод основан на изменении состояния ядра атома при взаимодействии с другими ядрами или частицами. Например, при бомбардировке атома нейтронами можно наблюдать различные ядерные реакции, которые могут быть использованы для определения количества нейтронов в атоме. |
| 3. Использование ядерной магнитной резонансной спектроскопии |
| Этот метод основан на измерении ядерного магнитного резонанса атома. Поскольку нейтроны имеют магнитный момент, их присутствие может привести к изменениям в спектре ядерного магнитного резонанса. Путем анализа этих изменений можно определить количество нейтронов в атоме. |
| 4. Использование методов дифракции |
| Этот метод основан на измерении дифракции излучения, проходящего через атом. Нейтроны принимают участие в дифракционных процессах и влияют на характер дифракционной картины. Путем анализа этой картины можно определить количество нейтронов в атоме. |
Выбор конкретного метода определения количества нейтронов в атоме зависит от условий исследования, доступных инструментов и требуемой точности результатов.
Применение полученной информации о количестве нейтронов

Знание количества нейтронов в атоме имеет важное значение в различных научных и технических областях. Вот некоторые способы использования этой информации:
1. Исследования ядерных реакций и распадов.
Количество нейтронов в атоме влияет на его стабильность и скорость распада. Ученые используют данный параметр для изучения ядерных реакций и распадов, что позволяет получить новые данные о свойствах различных элементов.
2. Изотопный анализ.
Изотопный анализ широко применяется в геологии, экологии и медицине. Количество нейтронов в атоме является основой для различия изотопов разных элементов. С помощью этой информации можно определить происхождение материалов, изучить изменения в окружающей среде или провести диагностику заболеваний.
3. Синтез новых материалов.
Изменение количества нейтронов в атоме позволяет создавать новые материалы с уникальными свойствами. Например, в ядерной энергетике, ученые исследуют различные изотопы для разработки новых топливных элементов и улучшения процесса деления атомов.
В результате использования полученной информации о количестве нейтронов в атоме, расширяется наше понимание мира и создаются новые возможности в различных сферах науки и технологии.