Вода с солью закипает быстрее - это одно из известных явлений, которое оказывает нас чересчур. Когда мы добавляем соль в кастрюлю с водой перед ее кипением, мы замечаем, что она начинает закипать гораздо раньше, чем обычно. Этот феномен вызывает много вопросов и вызывает интерес у ученых.
Чтобы понять, почему вода с солью закипает быстрее, необходимо обратиться к свойствам соли и их взаимодействию с молекулами воды. Соль, химический соединение, состоящее из ионов натрия (Na+) и ионов хлора (Cl-), влияет на физические свойства воды, особенно ее температуру кипения.
Когда соль попадает в воду, она диссоциирует, разделившись на положительные и отрицательные ионы. Этот процесс стимулирует колебательные движения молекул воды, что в свою очередь увеличивает их энергию. Повышение энергии молекул воды приводит к тому, что они начинают переходить в газообразное состояние раньше обычного.
Почему вода с солью закипает быстрее?

Соль является электролитом, то есть веществом, разлагающимся на ионы при растворении в воде. Когда соль растворяется в воде, ионы соли нарушают связи между молекулами воды, что приводит к повышению температуры кипения раствора.
Этот эффект известен как коллигативное свойство растворов и зависит от концентрации растворенных веществ. Чем больше концентрация соли в растворе, тем выше будет точка кипения.
Такое повышение точки кипения объясняется изменением химического потенциала растворителя - воды. Наличие соли влияет на количество свободных молекул воды, что требует большей энергии для перехода в парообразное состояние.
Таким образом, добавление соли в воду повышает точку кипения, что приводит к увеличению скорости закипания раствора по сравнению с обычной водой.
Влияние соли на свойства воды

Добавление соли в воду может изменить ее физические и химические свойства. Вот некоторые изменения, которые происходят при добавлении соли:
- Понижение температуры замерзания. Когда вода содержит соль, ее точка замерзания снижается. Это объясняет, почему соленая вода замерзает при более низкой температуре, чем пресная вода.
- Увеличение температуры кипения. Соль увеличивает температуру кипения воды, что означает, что вода с солью закипает быстрее, чем чистая вода. Это может быть полезно, например, при приготовлении пищи.
- Увеличение электропроводности. Соль в воде создает ионные соединения, которые повышают электропроводность воды. Это может иметь значение, например, при использовании воды в электролизе или для создания электролитических растворов.
- Изменение вкуса. Добавление соли может изменить вкус воды, делая ее соленой.
- Изменение pH-значения. Соли могут влиять на pH-значение воды, делая ее щелочной или кислой.
В целом, соль оказывает значительное влияние на свойства воды, что делает ее полезной в различных областях, таких как приготовление пищи, химическая и биологическая наука, а также водоснабжение и обработка сточных вод.
Молекулярное объяснение явления

Явление более быстрого кипения воды с добавленной солью может быть объяснено на молекулярном уровне. Когда соль растворяется в воде, происходит диссоциация, то есть разделение молекул соли на ионы. Например, в случае раствора кухонной соли (NaCl) в воде, одна молекула NaCl расщепляется на один ион натрия (Na+) и один ион хлорида (Cl-).
Ионы соли оказывают влияние на физические и химические свойства воды. В частности, высокая концентрация ионов в растворе приводит к увеличению количества столкновений между молекулами воды и ионами, что увеличивает скорость протекания реакций. Это объясняет более быстрое закипание воды.
Кроме того, ионы соли изменяют структуру воды. Обычно молекулы воды образуют клубки, называемые "агрегатами". Ионы соли притягивают молекулы воды и изменяют структуру агрегатов. Это приводит к снижению точки кипения воды с добавленной солью и соответственно ускоряет процесс кипения.
Наконец, соль также может способствовать образованию пузырьков водяного пара. Ионы соли могут быть запечатлены внутри пузырька, изменяя его поверхностное натяжение и ускоряя образование пара. Это также способствует более быстрому закипанию воды с солью.
Все эти процессы взаимодействия между ионами соли и молекулами воды объясняют, почему вода с солью закипает быстрее. Однако, следует отметить, что точное молекулярное объяснение явления все еще является предметом исследования и дискуссии.
Взаимодействие соли с молекулами воды
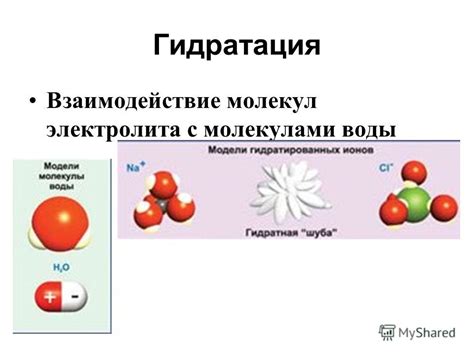
Когда соль растворяется, ионы соли разделяются на положительно заряженные катионы и отрицательно заряженные анионы. Водные молекулы образуют гидратные оболочки вокруг каждого иона соли. Гидратные оболочки позволяют эффективно передавать тепло между молекулами ионов соли.
Эти гидратные оболочки также уменьшают внутреннее трение между молекулами соли, позволяя им двигаться свободно в воде. Это является одной из причин, по которой вода с солью закипает быстрее. Молекулы соли ускоряют передачу тепла в воде и способствуют более эффективному движению молекул.
Другим фактором, который способствует более быстрому закипанию воды с солью, является электролитическое поведение ионов соли. Электролиты, такие как соль, способны проводить электрический ток. Когда вода нагревается, ионы соли усиливают электролитическое поведение и создают больше точек кипения воды. Это приводит к повышенному парообразованию и, следовательно, более быстрому закипанию.
Снижение плотности раствора
Раствор соли в воде имеет более высокую плотность по сравнению с чистой водой. Однако при нагревании плотность раствора снижается, что может быть одной из причин того, почему вода с солью закипает быстрее.
Когда вода нагревается, молекулы начинают двигаться более энергично. При этом происходит разбавление соли в растворе, так как молекулы соли начинают двигаться быстрее и отдают часть своей энергии молекулам воды. Это приводит к снижению количества соли в каждой частице раствора и, соответственно, к снижению плотности.
Снижение плотности раствора соли во время нагревания оказывает влияние на процесс кипения. Более низкая плотность солевого раствора делает его молекулы более подвижными, что облегчает их переход в паровую фазу. Пары могут образовываться легче и быстрее, чем в случае с чистой водой, и ускорять процесс кипения.
В то же время, чистая вода обладает более высокой плотностью при нагревании, что препятствует быстрому движению ее молекул и образованию паров. Поэтому, когда вода с солью и чистая вода нагреваются одновременно, раствор с солью начинает закипать быстрее.
Практическое применение и полезность

Изучение явления, при котором вода с солью закипает быстрее, имеет практическое применение в различных областях науки и техники. Ниже приведены некоторые примеры его полезности:
| Область | Применение |
|---|---|
| Кулинария | Использование соленой воды при варке яиц позволяет сделать более легко снимаемой скорлупу и предотвратить разрыв яйца в процессе варки. |
| Химия | Использование соленой воды при различных химических экспериментах ускоряет процессы реакции и обеспечивает более точные результаты. |
| Биология | Изучение влияния соленой воды на жизнедеятельность различных организмов позволяет лучше понять их адаптационные механизмы и выявить потенциальные применения в биотехнологии. |
| Теплотехника | Использование соленой воды в системах охлаждения и нагрева позволяет повысить эффективность и скорость работы таких систем. |
| Медицина | Исследование эффекта соленой воды на глаза и слизистые оболочки позволяет найти новые методы лечения различных заболеваний глаз и дыхательных путей. |
Таким образом, изучение и практическое применение явления, при котором вода с солью закипает быстрее, является важным исследованием, которое находит свое применение в различных областях науки и техники.