Фенол - это химическое соединение, которое широко используется в промышленности и научных исследованиях. Оно имеет много полезных свойств, и поэтому привлекает внимание ученых и инженеров. Изучение реакции фенола с щелочами является одним из важных аспектов его химии.
Первопричины реакции фенола с щелочами объясняются его молекулярной структурой. Фенол обладает ароматическим кольцом, где группа гидроксила (-OH) присоединена к бензольному кольцу. Группа гидроксила делает этот органический соединение более реакционноспособным по сравнению с бензеном.
Реакция фенола с щелочами, такими как натрия гидроксид (NaOH) или калия гидроксид (KOH), происходит путем замещения атома водорода в группе гидроксила. В результате этой реакции образуются соли фенолата и вода. Процесс следующий: гидроксид генерирует гидроксильную ион, который атакует атом водорода в гидроксильной группе фенола, образуя анион фенолата.
Реакция фенола с щелочами протекает с высокой степенью стереоспецифичности и селективности. Степень реакции зависит от концентрации щелочных реагентов, времени реакции и условий окружающей среды. Фенолаты могут претерпевать дальнейшие превращения, такие как окисление, ацилирование и аминирование, что делает реакцию фенола с щелочами значимой для производства различных органических соединений.
Фенол и его реакция с щелочами
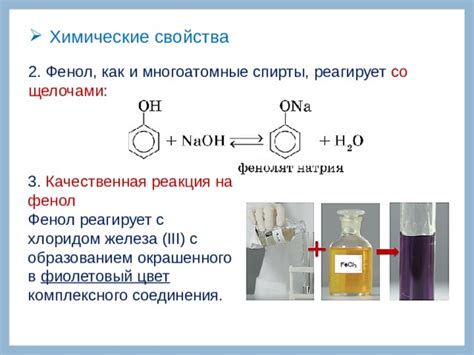
Реакция фенола с щелочами протекает по следующему механизму:
- Щелочь (NaOH, KOH) реагирует с фенолом, образуя анион фенолата.
- Полученный фенолат является более реакционноспособным, чем сам фенол и может участвовать в различных химических реакциях.
- Фенолат, например, может реагировать с другими соединениями, образуя сложные органические продукты.
Реакция фенола с щелочами имеет ряд особенностей:
- Реакция протекает при обычных условиях температуры и давления.
- Реакция является химический путем для получения многих фармацевтических и косметических продуктов.
- Реакция фенола с щелочами является реакцией нарастающей степени, то есть с увеличением количества щелочи возрастает количество образующегося фенолата.
- Реакция может сопровождаться выделением тепла и образованием газов, таких как водород.
Таким образом, реакция фенола с щелочами представляет собой важное химическое превращение, которое имеет широкое применение в промышленности и науке.
Химический состав и свойства фенола
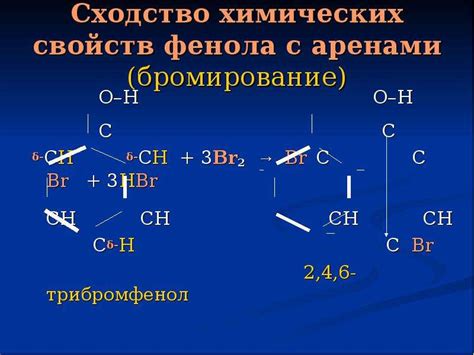
Фенол является бесцветной жидкостью с характерным запахом, легко смешивается с водой и большинством органических растворителей. Он обладает свойствами кислоты, реагируя с щелочами и образуя соли, такие как фенолаты.
Фенол обладает высокой реакционной способностью из-за наличия электронодонорной группы (-OH) и ароматического кольца. Эти химические особенности позволяют фенолу проводить реакции с различными реагентами и возможностями различными способами в синтезе органических соединений.
Свойства фенола также включают его способность окисляться, а также подвергаться нуклеофильной ароматической подстановке. Фенол также обладает антисептическими свойствами и широко используется в производстве различных химических соединений, включая пластмассы, лекарственные средства и красители.
Механизм реакции фенола с щелочами

Вначале происходит депротонирование фенола щелочью, такой как гидроксид натрия или гидроксид калия. Щелочная среда обладает высокой базичностью и может отбирать протон с молекулы фенола, образуя феноксид и ион гидроксида. Эта реакция является равновесной, но благодаря избытку щелочи, равновесие смещается в сторону продуктов.
Далее происходит протекание последующих реакций. Один из возможных путей - аддиция молекулы воды к феноксидному иону, что приводит к образованию спирта. Этот процесс является обратимым и может переходить в обратную сторону при сильном нагревании или разбавлении продукта.
Также существует возможность реакции феноксида с дополнительными молекулами щелочи, образуя анионат ион. Этот процесс полностью обратим и зависит от концентрации ионов в реакционной среде.
Механизм реакции фенола с щелочами имеет не только теоретическое значение, но и практическую применимость. Он используется для получения различных органических соединений, таких как спирты и анионы, а также для проведения определенных аналитических методик.
Причины реакции фенола с щелочами

Основными причинами реакции фенола с щелочами являются:
- Отрицательное ионное зарядов фенолатионов: При добавлении щелочи в водный раствор фенола, NaOH диссоциируется на ионы Na+ и OH-. Гидроксид-ионы (OH-) образуют отрицательно заряженный комплекс в результате отвлечения протона (H+) от фенола, сформировав образованный соединение, известное как основное фенолатион (C6H5O-).
- Удаление протона на ароматическом кольце: Протон, расположенный на ароматическом кольце фенола, является слабым кислотным центром. При взаимодействии с гидроксид-ионами, протон отдаётся на них, образуя нейтральный воду (H2O). Этот процесс называется вытеснением протона и является термодинамически выгодным, так как ОН- группа более базична, чем фенол.
- Образование солей фенолата: Результатом реакции фенола с щелочами является образование солей фенолатов. Фенолат-ионы (C6H5O-) образуют ионные связи с положительно заряженными ионами металлов (например, Na+), образующими фенолатную соль. Это обусловлено тем, что фенолатион-ионы являются кислотно-основными парами, которые соединяются с ионами металла, образуя стабильные соли.
Таким образом, реакция фенола с щелочами происходит путем образования отрицательно заряженных фенолатионов, способных образовывать соли с положительно заряженными металлическими ионами. Эта реакция является важным аспектом в химии фенола и имеет широкое применение в промышленных и медицинских процессах.
Физические и химические особенности реакции фенола с щелочами
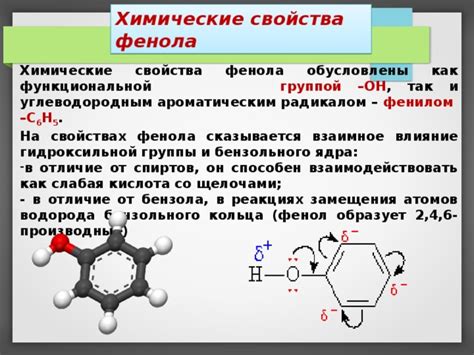
Одной из особенностей данной реакции является то, что фенол может образовывать стабильные соли с щелочными металлами, такими как натрий и калий. Это происходит в результате обменной реакции, при которой атомы водорода в молекуле фенола замещаются на металлы.
Физические особенности данной реакции связаны с изменениями во внешнем виде вещества. При взаимодействии фенола с щелочами образуется новое вещество, которое может иметь другой цвет и запах. Также может происходить образование осадка в результате выпадения несвязанной соляной кислоты.
Химические особенности реакции зависят от концентрации фенола и щелочи, а также от условий проведения реакции. При повышенной концентрации фенола и щелочи реакция может протекать более интенсивно и быстро. Также важным фактором является температура реакции, которая может влиять на скорость и характер образования продуктов.
Важно отметить, что реакция фенола с щелочами является реакцией обратимой. Это означает, что можно достичь равновесия между продуктами и исходными веществами. При этом, если изменить условия реакции, например, изменить концентрацию одного из реагентов или температуру, то равновесие может сместиться в сторону образования других продуктов.
Применение реакции фенола с щелочами

Реакция фенола с щелочами имеет широкое применение в различных областях химии и промышленности. Особенности этой реакции делают ее полезным инструментом для получения различных продуктов и соединений.
В фармацевтической промышленности, реакция фенола с щелочами используется для получения различных лекарственных препаратов. Фенол является важным промежуточным продуктом при синтезе анальгетиков, антипиретиков и других медицинских препаратов. Благодаря способности фенола образовывать стабильные соли с щелочами, его можно использовать для получения стабильных и эффективных форм лекарственных веществ. За счет этого, фенол широко применяется в процессе синтеза и производства лекарственных препаратов.
Кроме того, реакция фенола с щелочами используется в примыкании материалов в производстве различных пластмасс и синтетических материалов. Фенол, после взаимодействия с щелочами, образует стабильные соединения, которые имеют высокую термостойкость и механическую прочность. Поэтому, эти соединения часто используются в качестве связующего агента или добавки в производстве пластиков, клеев и лаков.
Кроме того, реакция фенола с щелочами используется в качестве метода очистки и дезинфекции различных поверхностей. Фенол имеет сильное антисептическое действие и широко применяется в медицине и гигиене. Фенол, образующийся при реакции с щелочами, обладает высокой бактерицидной активностью и может быть использован для дезинфекции поверхностей, инструментов и оборудования в медицинских и лабораторных учреждениях.
Таким образом, реакция фенола с щелочами имеет широкое применение в различных сферах человеческой деятельности. Она является важным инструментом для получения различных продуктов и соединений, а также для обработки и очистки различных поверхностей. Применение этой реакции позволяет получить стабильные, эффективные и безопасные вещества, которые находят свое применение в различных отраслях промышленности и науки.