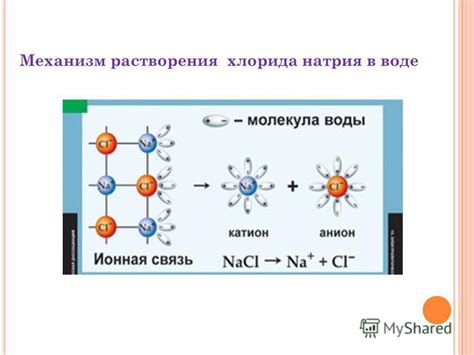
Хлорид натрия, более известный как обычная кухонная соль, является одним из самых распространенных химических соединений на земле. Под воздействием воды эти мелкие кристаллы легко растворяются, превращаясь в ионы натрия (Na+) и ионы хлорида (Cl-).
Растворение хлорида натрия в воде играет ключевую роль в нашей жизни. Вода является универсальным средством для растворения различных веществ, и раствор хлорида натрия не является исключением. Растворенная соль важна для многих процессов, происходящих в нашем организме.
Чрезвычайно важной ролью растворенной соли является поддержание жизненно важного баланса электролитов в нашем организме. Электролиты - это электрически заряженные частицы, которые могут находиться как внутри клеток, так и во внеклеточной жидкости. Натрий и хлорид являются двумя из наиболее распространенных электролитов в организме человека.
Благодаря своей растворимости хлорид натрия продолжает играть важнейшую роль в различных областях: от пищевой промышленности до медицины. Он используется для обработки и консервации пищевых продуктов, приготовления лекарств, стерилизации инструментов в медицинских учреждениях и многого другого.
Важность растворения хлорида натрия в воде
Одной из основных причин важности растворения хлорида натрия в воде является его роль в поддержании гомеостаза в клетках организма. Хлорид натрия играет важную роль в биохимических процессах, таких как передача нервных импульсов, сокращение мышц и усвоение пищи. Растворение хлорида натрия в воде помогает поддерживать электролитный баланс организма и обеспечивает нормальное функционирование клеток.
Растворение хлорида натрия также имеет важное значение в промышленности. В процессе производства многих химических веществ, лекарств, пластиков и стекла требуется использование растворов хлорида натрия. Кроме того, хлорид натрия используется как ингредиент в пищевой промышленности, в производстве консервации, соленых орехов, мясных продуктов и сыров.
Не менее важна роль хлорида натрия в области сельского хозяйства и экологии. Растворы хлорида натрия используются для орошения почв, дезинфекции воды в бассейнах и водоемах, а также для уменьшения образования льда на дорогах в холодные периоды года. Таким образом, растворение хлорида натрия в воде способствует повышению урожайности, обеспечению безопасности и сохранению окружающей среды.
В итоге, растворение хлорида натрия в воде имеет огромную важность и используется во многих сферах нашей жизни. Это позволяет поддерживать нормальные жизненные процессы в организме, производить различные химические вещества, обеспечивать безопасность и улучшать качество нашей жизни в целом.
Химические свойства и структура хлорида натрия

Одним из главных свойств хлорида натрия является его способность растворяться в воде. Вода - полярное вещество, а ионы в хлориде натрия имеют полярность. Ионы Na+ обладают положительным зарядом, а ионы Cl- - отрицательным зарядом. Вода молекулярно связана с ионами, притягивая их частички к себе и разделяя их.
Структура хлорида натрия имеет кристаллическую форму. Каждый ион натрия окружен шестью ионами хлора, а каждый ион хлора окружен шестью ионами натрия. Это создает трехмерную решетку, в которой ионы удерживаются вместе. Кристаллическая структура делает хлорид натрия твердым и хрупким веществом при комнатной температуре.
Хлорид натрия также обладает химической реакционной активностью. Он может образовывать два типа соединений - карбонат и гидрат. Карбонат натрия (Na2CO3), также известный как пищевая сода или пищевой гидрат натрия (Na2CO3•10H2O), часто используется в пищевой промышленности как подкислитель и растворитель.
Хлорид натрия также является электролитом и проводит электрический ток в растворе. Когда хлорид натрия растворяется в воде, ионы Na+ и Cl- свободно перемещаются в растворе, позволяя электрическому току проходить. Это свойство делает хлорид натрия полезным в многих технических, медицинских и научных приложениях.
Полярность молекулы воды и растворение веществ
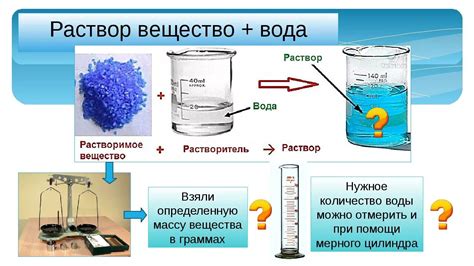
Молекула воды состоит из двух атомов водорода и одного атома кислорода, соединенных ковалентными связями. Кислород притягивает электроны сильнее, чем водород, создавая разделение зарядов в молекуле. В результате, молекула воды становится полярной.
Полярность молекулы воды приводит к образованию в воде диполя. Это означает, что вода имеет отрицательно заряженную часть (кислород) и положительно заряженную часть (водород), которые притягивают другие полярные молекулы.
Когда вещество растворяется в воде, положительно и отрицательно заряженные части молекулы растительного или ионного вещества взаимодействуют с отрицательно и положительно заряженными частями молекулы воды. Это позволяет веществу разделить на мельчайшие частицы и равномерно распределиться по объему раствора.
Полярность молекулы воды также обеспечивает способность взаимодействия с молекулами других веществ, включая неполярные молекулы. Это объясняет, почему хлорид натрия, который является молекулой с ионными связями, может раствориться в воде и образовать раствор с положительно заряженными натриевыми и отрицательно заряженными хлоридными ионами.
Таким образом, полярность молекулы воды играет важную роль в процессе растворения веществ, позволяя им полностью смешиваться и распределяться в растворе.
Процесс растворения хлорида натрия в воде
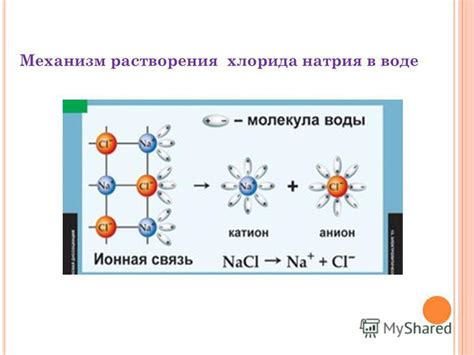
Вода - универсальный растворитель, способный растворять в себе множество различных веществ. Когда хлорид натрия добавляется в воду, его молекулы или ионы распадаются на положительно заряженные ионы натрия (Na+) и отрицательно заряженные ионы хлорида (Cl-).
Молекулы воды являются полярными, у них есть электрический дипольный момент. Этот дипольный момент позволяет молекулам воды взаимодействовать с ионами хлорида натрия. Положительно заряженные ионы натрия притягиваются к отрицательным кислородным атомам молекул воды, а отрицательно заряженные ионы хлорида - к положительно заряженным водородным атомам.
В результате этих притяжений ионов и молекул воды образуется гидратная оболочка вокруг каждого иона хлорида натрия. Образовавшиеся гидраты очень стабильны и эффективно разбивают солидную решетку кристаллической структуры хлорида натрия, обеспечивая полное растворение в воде.
Процесс растворения хлорида натрия в воде сопровождается выделением или поглощением тепла (эндотермный или экзотермный процесс), что зависит от условий и концентрации раствора. При осаждении хлорида натрия из раствора происходит обратный процесс - ионы хлорида натрия снова стремятся объединиться в солидную кристаллическую форму.
Раствор хлорида натрия находит применение во многих сферах наук и технологий, включая химическую промышленность, медицину, пищевую промышленность и другие. Знание процесса растворения хлорида натрия в воде позволяет лучше понять физико-химические свойства этого вещества и его применение в различных областях.
Ключевые роли, которые играет растворенный хлорид натрия

Хлорид натрия, также известный как поваренная соль, широко используется в пищевой промышленности и в медицине. Когда хлорид натрия растворяется в воде, он играет несколько ключевых ролей, которые важны для нашего организма и окружающей среды.
Одна из главных ролей растворенного хлорида натрия состоит в поддержании электролитного баланса в нашем организме. Электролиты - это минералы, которые имеют положительный или отрицательный заряд и играют важную роль в регуляции различных процессов в нашем организме, включая работу сердца, мышц и нервов. Распределение электролитов внутри и вне клеток организма контролируется концентрацией растворенного хлорида натрия.
Кроме того, растворенный хлорид натрия имеет антисептические свойства, которые помогают предотвращать рост и размножение бактерий в воде. Это делает его полезным ингредиентом для дезинфекции воды, использования в медицине и в процессе очистки ран, чтобы предотвратить инфекцию.
Растворенный хлорид натрия также играет важную роль в нашей пище. Он служит не только для усиления вкуса и поддержания требуемого уровня солености, но также является необходимым элементом для правильного функционирования нервной системы и мышц. Он помогает поддерживать нормальное кровяное давление и регулирует баланс жидкостей в организме.
| Роли растворенного хлорида натрия: |
|---|
| - Поддержание электролитного баланса |
| - Антисептические свойства |
| - Регуляция вкуса и солености еды |
| - Лечение ран и предотвращение инфекции |
| - Регулирование нервной системы и мышц |
| - Поддержание нормального кровяного давления |
| - Регулирование баланса жидкостей в организме |
Влияние растворения хлорида натрия на свойства воды
Растворение хлорида натрия в воде играет ключевую роль во многих ее свойствах. Этот процесс приводит к образованию ионов натрия (Na+) и хлорида (Cl-) в растворе.
Ионы Na+ и Cl- обладают свойством образовывать электрически нейтральные соединения, что приводит к повышению электропроводности воды. Это возможно из-за того, что ионы хлорида и натрия являются электролитами, такими как соль.
Кроме того, растворение хлорида натрия в воде приводит к изменению плотности воды. В итоге, раствор хлорида натрия имеет более высокую плотность по сравнению с чистой водой. Это свойство имеет значение, например, для плавания, так как благодаря растворению хлорида натрия вода становится плотнее и позволяет лучше поддерживать тело на поверхности.
Кроме того, растворение хлорида натрия в воде влияет на ее температуру плавления и кипения. Вода с растворенным хлоридом натрия имеет более низкую температуру плавления и более высокую температуру кипения. Это является результатом нарушения водородных связей между молекулами воды.
Таким образом, растворение хлорида натрия в воде не только увеличивает электропроводность, но и изменяет физические свойства воды, что придает ей уникальные свойства и широко используется в различных областях науки и технологий.
Важность растворения хлорида натрия для организма

Регуляция водного баланса: Растворение хлорида натрия в воде позволяет организму поддерживать правильный уровень влаги. Натрий притягивает воду и помогает поддерживать оптимальную концентрацию внутриклеточного и внеклеточного жидкостей.
Нервная система и мышцы: Натрий является ключевым элементом для проведения электрических импульсов в нервных клетках. Этот элемент необходим для нормальной работы нервной системы и мышц, включая сердечную мышцу.
Регуляция кислотно-щелочного баланса: Хлорид натрия помогает поддерживать оптимальный уровень pH в организме, обеспечивая буферную систему для регулирования кислотности. Он также влияет на процесс пищеварения, помогая образованию и выработке соляной кислоты в желудке.
Транспорт кислорода и питательных веществ: Хлорид натрия играет важную роль в процессе транспортировки кислорода и питательных веществ в организме. Он помогает поддерживать правильный уровень вязкости крови, что способствует нормальной циркуляции и доставке кислорода и питательных веществ к клеткам и тканям.